题目内容
下列物质混合后不能生成氢氧化钠的是( )
| A、Ba(OH)2 和Na2CO3溶液 |
| B、Na和H2O |
| C、KOH和NaCl溶液 |
| D、Na2O2和H2O |
考点:钠的化学性质,钠的重要化合物
专题:元素及其化合物
分析:A.Ba(OH)2 和Na2CO3溶液反应生成碳酸钡和氢氧化钠;
B.Na和H2O反应生成氢氧化钠和氢气;
C.KOH和NaCl溶液不反应;
D.Na2O2和H2O反应生成氢氧化钠和氧气.
B.Na和H2O反应生成氢氧化钠和氢气;
C.KOH和NaCl溶液不反应;
D.Na2O2和H2O反应生成氢氧化钠和氧气.
解答:
解:A.Ba(OH)2 和Na2CO3溶液反应的化学方程式:Ba(OH)2+Na2CO3=BaCO3↓+2NaOH,故A正确;
B.Na和H2O反应的方程式为:2Na+2H2O═2NaOH+H2↑,故B正确;
C.KOH和NaCl溶液不复合离子反应的条件,不反应,故C错误;
D.Na2O2和H2O反应的方程式为:2Na2O2+2H2O═4NaOH+O2↑,故D正确;
故选:C.
B.Na和H2O反应的方程式为:2Na+2H2O═2NaOH+H2↑,故B正确;
C.KOH和NaCl溶液不复合离子反应的条件,不反应,故C错误;
D.Na2O2和H2O反应的方程式为:2Na2O2+2H2O═4NaOH+O2↑,故D正确;
故选:C.
点评:本题考查了氢氧化钠的制备,熟悉钠及其化合物的性质是解题关键,注意离子反应的条件,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列溶液中Cl-浓度最小的是( )
| A、200ml 3mol/L MgCl2溶液 |
| B、1000ml 4mol/L NaCl溶液 |
| C、300ml 5mol/L KCL溶液 |
| D、1000ml 1mol/L AlCl3溶液 |
下列物质中属于非电解质的是( )
| A、盐酸 |
| B、氨水 |
| C、H2SO4 |
| D、SO3 |
下列溶液中的物质的量浓度为1mol/L的是( )
| A、将22.4 L氯化氢气体溶于水配成1 L溶液 |
| B、将40 g NaOH溶于1L水中配成溶液 |
| C、从1 L 1 mol/L的NaOH溶液中取出50 mL,则取出的溶液中溶质的物质的量浓度 |
| D、将1 L 10 mol/L的浓盐酸与9 L水混合 |
氮化钠和氢化钠都是离子化合物,与水反应的化学方程式(未配平)如下:
Na3N+H2O→NaOH+NH3
NaH+H2O→NaOH+H2
有关它们的叙述正确的是( )
Na3N+H2O→NaOH+NH3
NaH+H2O→NaOH+H2
有关它们的叙述正确的是( )
| A、离子半径:N3->Na+>H+ |
| B、与水反应都是氧化还原反应 |
| C、与盐酸反应都只生成一种盐 |
| D、两种化合物中的阴阳离子均具有相同的电子层结构 |
下列试剂都能与抗酸药的有效成分反应的是( )
| A、盐酸 | B、氢氧化钠 |
| C、氯化铝 | D、碳酸 |
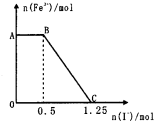 已知酸性高锰酸钾溶液可以将FeS04氧化,方程式为2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )
已知酸性高锰酸钾溶液可以将FeS04氧化,方程式为2KMnO4+10FeSO4+8H2SO4═K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,则下列有关说法不正确的是( )| A、图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B、图中BC段发生的反应为2Fe3++2I-═2Fe2++I2 |
| C、向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
| D、根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol |
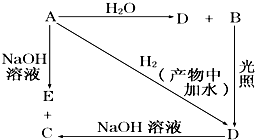 常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示.
常温下,A是可用来对自来水进行消毒的黄绿色气体单质,A、B、C、D、E都含X元素,其转化关系如图所示.