题目内容
7.非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成: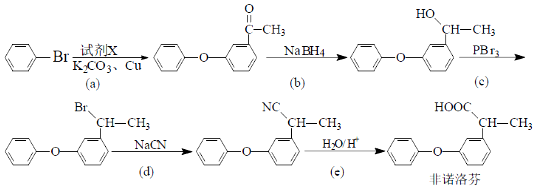
①反应中加入的试剂X的分子式为C8H8O2,X的结构简式为
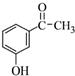 .
.②上述反应中是取代反应的有acd(填字母),是还原反应的有b(填字母).
③非诺洛芬的一种同分异构体满足下列条件,写出该异构体的结构简式:
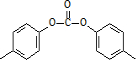 .
.I不能与FeCl3发生显色反应,但其一种水解产物能与FeCl3发生显色反应.
II分子中有3种不同化学环境的氢,且分子中含有两个苯环.
分析 ①X的分子式为C8H8O2,由反应前后有机物的结构可知,X含苯环,且苯环的间位上有-OH、-COCH3;
②由结构中官能团的变化可知,acd为取代反应,b为加成反应,e为水解反应;
③非诺洛芬的一种同分异构体满足I不能与FeCl3发生显色反应,但其一种水解产物能与FeCl3发生显色反应,则不含酚-OH,水解产物含酚-OH;
II分子中有3种不同化学环境的氢,且分子中含有两个苯环,结构对称,含3种H,以此来解答.
解答 解:①对比反应a中反应物、产物结构、X的分子式,可知发生取代反应,还生成HBr,可知X的结构简式为 ,故答案为:
,故答案为: ;
;
②对比反应中反应物、生成物结构简式,可知反应a属于取代反应,反应b中是羰基转化为羟基,获得氢,属于还原反应,反应c中是-OH被-Br取代,反应d中-Br被-CN取代,均属于取代反应,反应e中-CN转化为-COOH,属于水解反应,
故答案为:acd;b;
③非诺洛芬的一种同分异构体满足I不能与FeCl3发生显色反应,但其一种水解产物能与FeCl3发生显色反应,则不含酚-OH,水解产物含酚-OH;
II分子中有3种不同化学环境的氢,且分子中含有两个苯环,结构对称,含3种H,该异构体的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的合成,为高频考点,把握合成流程中官能团的变化、官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意同分异构体书写为解答的难点,题目难度较大.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
17.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 室温下,pH=12的NaAlO2溶液中,由水电离得OH-数目为0.01NA | |
| B. | 常温常压下,N2H4和CH3OH的混合物64g含有12NA个原子 | |
| C. | 0.1molCl2全部溶于水后转移电子的数目为0.1NA | |
| D. | 苯与液溴反应生成1mol溴苯,消耗0.5NA个Br2 |
18.下列有关有机化合物的说法正确的是( )
| A. | 乙烯分子中碳碳键的键能是乙烷分子中碳碳键的2倍,因而乙烯比乙烷稳定 | |
| B. | 石油裂化的目的是为了将直链烃转化为芳香烃 | |
| C. | 分子式为C4H8O2的有机物,存在含有六元环的同分异构体 | |
| D. | 有机物  不能发生氧化反应,但可以发生消去反应、取代反应和加成反应 不能发生氧化反应,但可以发生消去反应、取代反应和加成反应 |
15.下列生活中常见物质的用途与其还原性有关的是( )
| A. |  碘酒中的碘 | B. |  暖宝宝中的铁粉 | ||
| C. |  抗酸药中的氢氧化铝 | D. |  尿不湿中的聚丙烯酸钠 |
2.X、Y、Z、W是核电荷数依次增大的四种短周期主族元素,已知Z的单质固体显黄色,Y能形成两种液态氢化物M、Q,其中Q具有漂白性,X能形成多种单质,其中有一种是常用的导体材料,下列说法中错误的是( )
| A. | 非金属性:Y>W>Z | |
| B. | 将W的单质通入M中可得到具有漂白性的溶液 | |
| C. | 四种元素的常见单质中X的单质的沸点最高 | |
| D. | 最高正价氧化物对应水化物酸性强弱:X>Z>W |
12.下列各组离子在相应的条件下可能大量共存的是( )
| A. | pH=1的溶液中:CO32-、K+、Cl-、Na+ | |
| B. | 由水电离产生的c(OH-)=1×10-13mol•L-1的溶液中:NO3-、Mg2+、Na+、SO42- | |
| C. | 在$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×1012的溶液中:NH4+、Fe2+、Cl-、NO3- | |
| D. | 含Al3+的溶液中:Na+、HCO3-、Cl-、K+ |
19.CH2=CH2与H2反应的能量与反应进程关系如图所示.下列说法错误的是( )

| A. | 该反应为放热反应 | |
| B. | 催化剂Ⅱ比催化剂Ⅰ活性更好 | |
| C. | 催化剂可改变反应的活化能和焓变 | |
| D. | 正反应的活化能小于逆反应的活化能 |
5.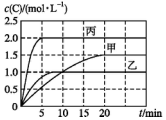 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:
下列说法正确的是( )
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间的变化关系分别以表和图表示:| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | 1.0 L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6.0 mol A 2.0 mol B |
| A. | 10 min内甲容器中反应的平均速率v(A)=0.025 mol•L-1•min-1 | |
| B. | 由图可知:T1<T2,该反应为吸热反应 | |
| C. | x=1,若平衡时保持温度不变,改变容器体积平衡不移动 | |
| D. | T2℃时,丙容器比乙容器反应快的原因是使用了催化剂 |
6.下列有关性质的比较正确的是( )
| A. | 原子半径:P<S<Cl | B. | 非金属性:P>S>Cl | ||
| C. | 酸性:H3PO4<H2SO4<HClO4 | D. | 稳定性:PH3>H2S>HCl |