题目内容
17.向500mL NaOH溶液中投入10.8g Al,两者恰好完全反应,计算:(1)Al的物质的量.
(2)参加反应的NaOH的物质的量和溶液的物质的量浓度.
(3)生成的H2在标准状况下的体积.
分析 (1)根据n=$\frac{m}{M}$计算Al的物质的量;
(2)发生反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据方程式计算NaOH的物质的量,根据c=$\frac{n}{V}$计算其物质的量浓度;
(3)根据方程式计算氢气的物质的量,再根据V=n•Vm计算其体积.
解答 解:(1)10.8gAl的物质的量为:$\frac{10.8g}{27g/mol}$=0.4mol,
答:10.8gAl的物质的量为0.4mol;
(2)设参加反应的NaOH的物质的量为x mol,则:
2Al+2H2O+2NaOH=2NaAlO2+3H2↑
2 2
0.4mol xmol
则:2:2=0.4mol:x mol,解得:x=0.4,
故NaOH溶液的物质的量浓度为:$\frac{0.4mol}{0.5L}$=0.8mol/L,
答:参加反应的NaOH的物质的量为0.4mol,NaOH溶液的物质的量浓度为0.8mol/L;
(3)设生成氢气的物质的量为y mol,则:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2 3
0.4mol ymol
则:2:3=0.4mol:y mol,解得:y=0.6,
所以生成氢气在标准状况下的体积为:0.6mol×22.4L/mol=13.44L,
答:生成氢气的体积为13.44L.
点评 本题考查了化学方程式的计算,题目难度不大,明确发生反应的实质为解答关键,注意掌握物质的量与气体摩尔体积、摩尔质量之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列化学用语中,正确的是( )
| A. | 氯化钠的电子式为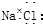 ? ? | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 氯化氢分子的形成过程可用电子式表示为:H×+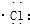 → →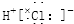 | |
| D. | 重水的化学式为${\;}_{1}^{2}$H2O(或D2O) |
12.下列有关蒸馏的实验装置与操作的说法中,不正确的是( )
| A. | 烧瓶必须垫石棉网加热 | |
| B. | 冷凝管中的水流是从下口进入,上口排出 | |
| C. | 实验中需要在烧瓶中加入几粒碎瓷片,防止出现暴沸现象 | |
| D. | 温度计的水银球应插入烧瓶中的液面以下 |
2.下列电离方程式正确的是( )
| A. | Al2(SO4)3═2Al3++3SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | Ba(OH)2═Ba2++(OH-)2 | D. | Na2SO3═Na++SO32- |
9.人的机体活动和维持恒定体温需要能量,下列物质主要为人体提供能量的是( )
| A. | 无机盐 | B. | 水 | C. | 糖类 | D. | 维生素 |
6.将1mol CO与1mol CO2相比较,正确的是( )
| A. | 分子数相等 | B. | 原子数相等 | C. | 电子数相等 | D. | 质子数相等 |
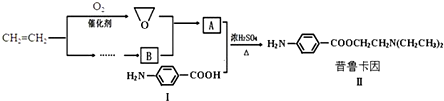

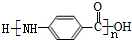 .
.
 .
. .F1和F2的关系为同分异构体.
.F1和F2的关系为同分异构体. ,二烯烃的通式是CnH2n-2.
,二烯烃的通式是CnH2n-2. CH3OH(g)
CH3OH(g)