题目内容
4.甲、乙两个烧瓶收集等量的NO2气体并密封,又知2NO2?N2O4△H<0,将甲置于热水中,乙置于冷水中.下列有关现象描述中正确的是( )| A. | 甲颜色加深 | B. | 乙颜色加深 | C. | 甲、乙颜色都加深 | D. | 甲、乙颜色都变浅 |
分析 可逆反应2NO2?N2O4,正反应放热,升高温度,化学平衡向逆反应方向移动,降低温度,平衡正向移动,以此解答该题.
解答 解:2NO2?N2O4 △H<0,将甲置于热水中,温度升高,平衡逆向移动,则二氧化氮的浓度增大,颜色加深,乙置于冷水中,温度降低,平衡正向移动,二氧化氮浓度降低,则颜色变浅,只有A正确.
故选A.
点评 本题考查化学平衡的影响,为高频考点,侧重考查学生的分析能力,注意把握温度对平衡移动的影响,把握二氧化氮的性质,难度不大.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
13.设NA为阿伏加德罗常数的值,下列叙述错误的是( )
| A. | 分子总数为NA的SO2和CO2的混合气体中含有的氧原子数为2NA | |
| B. | 0.1mol/L(NH4)2SO4溶液与0.2mol/LNH4Cl溶液中的NH4+数目相同 | |
| C. | 标准状况下,H2和CO混合气体8.96L在足量O2中充分燃烧消耗O2分子数为0.2NA | |
| D. | 1molNa与足量O2反应生成了混合物,Na失去NA个电子 |
14.短周期元素X、Y、Z、W的原子半径依次增大,其简单氢化物中X、Y、Z、W的化合价如表所示:
下列说法正确的是( )
| 元素 | X | Y | Z | W |
| 化合价 | -1 | -2 | -2 | -3 |
| A. | 最高价氧化物对应水化物的酸性:W>Z | |
| B. | 元素的非金属性:X>Y | |
| C. | 氢化物的沸点:Z>Y | |
| D. | 元素Y不存在同素异形现象 |
11.化学与人类的生活、生产密切相关,下列说法不正确的是( )
| A. | 船舶外壳装上锌块,是利用牺牲阳极的阴极保护法进行金属防腐 | |
| B. | 埃博拉病毒可用乙醇、次氯酸钠溶液、双氧水消毒,其消毒原理相同 | |
| C. | 压缩天然气(CNG)、液化石油气(LPG)的主要成分是烃类,是城市推广的淸洁燃料 | |
| D. | 2016年9月,中国太钢集团造出的圆珠笔头,可完全替代进口笔尖,该笔尖钢为合金,且具有良好的切削性 |
18. 其他条件不变时,改变密闭容器中某一条件,对反应A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所 示的曲线(T 表示温度,n 表示物质的量).下列判断正确的是( )
其他条件不变时,改变密闭容器中某一条件,对反应A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所 示的曲线(T 表示温度,n 表示物质的量).下列判断正确的是( )
 其他条件不变时,改变密闭容器中某一条件,对反应A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所 示的曲线(T 表示温度,n 表示物质的量).下列判断正确的是( )
其他条件不变时,改变密闭容器中某一条件,对反应A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所 示的曲线(T 表示温度,n 表示物质的量).下列判断正确的是( )| A. | 若 T1>T2,则正反应是吸热反应 | |
| B. | 达到平衡时,A2转化率:b>a>c | |
| C. | 在 T2和起始 n(A2)不变时达到平衡,n(AB3)大小为:c>b>a | |
| D. | 若 T2>T1,达到平衡时 b、d 两点的反应速率为:d>b |
16.有机物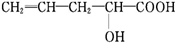 在不同条件下至少可能发生六种不同类型的有机反应:①加成;②取代;③消去;④氧化;⑤酯化;⑥加聚.其中由于分子结构中含-OH可能发生的反应有( )
在不同条件下至少可能发生六种不同类型的有机反应:①加成;②取代;③消去;④氧化;⑤酯化;⑥加聚.其中由于分子结构中含-OH可能发生的反应有( )
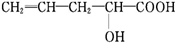 在不同条件下至少可能发生六种不同类型的有机反应:①加成;②取代;③消去;④氧化;⑤酯化;⑥加聚.其中由于分子结构中含-OH可能发生的反应有( )
在不同条件下至少可能发生六种不同类型的有机反应:①加成;②取代;③消去;④氧化;⑤酯化;⑥加聚.其中由于分子结构中含-OH可能发生的反应有( )| A. | ①④⑥ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | ①②③④ |
13.下列实验过程中,始终无明显现象的是( )
| A. | CO2通入CaCl2溶液中 | B. | NO2通入FeSO4溶液中 | ||
| C. | 乙烯通入溴的CCl4溶液中 | D. | SO2通入Ba(NO3)2溶液中 |
14.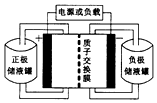 一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液.电池中发生的反应为2VCl2+BrCl${\;}_{2}^{-}$$?_{放电}^{充电}$2VCl3+Br-下列说法正确的是( )
一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液.电池中发生的反应为2VCl2+BrCl${\;}_{2}^{-}$$?_{放电}^{充电}$2VCl3+Br-下列说法正确的是( )
 一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液.电池中发生的反应为2VCl2+BrCl${\;}_{2}^{-}$$?_{放电}^{充电}$2VCl3+Br-下列说法正确的是( )
一种钒-多卤化物电池结构示意图如图所示,电池和储液罐均存储有反应物和酸性电解质溶液.电池中发生的反应为2VCl2+BrCl${\;}_{2}^{-}$$?_{放电}^{充电}$2VCl3+Br-下列说法正确的是( )| A. | VCl2存储在正极储液罐内 | |
| B. | 放电时H+从负极区移至正极区 | |
| C. | 充电时电池的负极与电源的正极相连 | |
| D. | 充电时阳极反应为Br-+2Cl--2e-═BrCl2- |
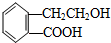 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.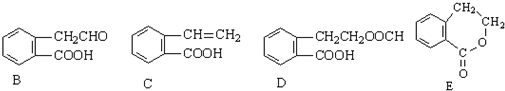
 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O.
+2H2O. .
.