题目内容
20.燃烧11.2L(标准状况)甲烷,生成二氧化碳和水的物质的量各是多少?分析 根据n=$\frac{V}{{V}_{m}}$计算11.2L甲烷的物质的量,再根据方程式CH4+O2$\stackrel{点燃}{→}$CO2+2H2O计算燃烧生成二氧化碳和水的物质的量.
解答 解:标况下,n(CH4)=$\frac{11.2L}{22.4L/mol}$=0.5mol,
设甲烷完全燃烧生成二氧化碳、水的物质的量分别为x、y,
CH4+O2$\stackrel{点燃}{→}$CO2+2H2O
1 1 2
0.5mol x y
所以,1:1=0.5mol:x,解得:x=0.5mol,
1:2=0.5mol:y,解得:y=1mol,
答:燃烧11.2L(标准状况)甲烷生成0.5mol二氧化碳、1mol水.
点评 本题考查了化学方程式的计算,题目难度不大,明确发生反应原理为解答关键,注意掌握物质的量与气体摩尔体积之间的关系,试题有利于培养学生的分析能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.CH2=CH-CH3加聚反应的产物是( )
| A. | 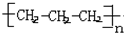 | B. | 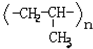 | C. | 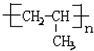 | D. | CH2=CH2 |
7.下列离子组一定能大量共存的是( )
| A. | 甲基橙呈黄色的溶液中:I-、Cl-、NO${\;}_{3}^{-}$、Na+ | |
| B. | 石蕊呈蓝色的溶液中:Na+、AlO${\;}_{2}^{-}$、NO${\;}_{3}^{-}$、HCO${\;}_{3}^{-}$ | |
| C. | 含大量Al3+的溶液中:K+、Na+、NO${\;}_{3}^{-}$、ClO- | |
| D. | 含大量OH-的溶液中:CO${\;}_{3}^{2-}$、Cl-、F-、K+ |
8.化学与生活密切相关.下列说法正确的是( )
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 乙烯可作水果的催熟剂 | |
| C. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
10.有关常温下pH均为3的硫酸和醋酸溶液的说法正确的是( )
| A. | 分别加水稀释100倍后,硫酸溶液的pH变化比醋酸溶液小 | |
| B. | 两种溶液中,由水电离出的c(H+)=1×10-11mol•L-1 | |
| C. | 与pH=11的NaOH溶液等体积混合后,都恰好中和 | |
| D. | 分别加入足量锌片充分反应后,两溶液中产生的氢气一样多 |