题目内容
某无色透明的溶液,能使石蕊变红,也能使酚酞变红的溶液中都能大量共存的是( )
| A、Fe3+ K+ SO42- NO3- |
| B、Mg2+NH4+ SO42- Cl- |
| C、Na+ K+ SO42- NO3- |
| D、K+ Na+ MnO4- SO42- |
考点:离子共存问题
专题:
分析:无色溶液中不存在Cu2+、Fe2+、Fe3+、MnO4-等有色离子,能使石蕊变红,溶液中存在大量氢离子,能使酚酞变红的溶液为碱性溶液,
A.铁离子为有色离子,且铁离子能够与碱性溶液中的氢氧根离子反应;
B.镁离子、铵根离子与碱性溶液中的氢氧根离子反应;
C.Na+ K+ SO42- NO3-离子之间不发生反应,且为无色离子,都不与氢离子和氢氧根离子反应;
D.高锰酸根离子为有色离子,不满足溶液无色的条件.
A.铁离子为有色离子,且铁离子能够与碱性溶液中的氢氧根离子反应;
B.镁离子、铵根离子与碱性溶液中的氢氧根离子反应;
C.Na+ K+ SO42- NO3-离子之间不发生反应,且为无色离子,都不与氢离子和氢氧根离子反应;
D.高锰酸根离子为有色离子,不满足溶液无色的条件.
解答:
解:A.Fe3+为有色离子,不满足溶液无色的条件,Fe3+能够与碱性溶液中的氢氧根离子反应生成氢氧化铁,在溶液中不能大量共存,故A错误;
B.Mg2+NH4与碱性溶液中的氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.Na+ K+ SO42- NO3-离子之间不反应,都是为无色离子,且都不与H+和OH-反应,在溶液中能够大量共存,故C正确;
D.MnO4-为有色离子,不满足溶液无色的要求,在溶液中不能大量存在,故D错误;
故选C.
B.Mg2+NH4与碱性溶液中的氢氧根离子反应,在溶液中不能大量共存,故B错误;
C.Na+ K+ SO42- NO3-离子之间不反应,都是为无色离子,且都不与H+和OH-反应,在溶液中能够大量共存,故C正确;
D.MnO4-为有色离子,不满足溶液无色的要求,在溶液中不能大量存在,故D错误;
故选C.
点评:本题考查离子共存的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
下列实验可达到实验目的是( )
A、将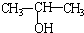 与NaOH的醇溶液共热制备CH3-CH═CH2 与NaOH的醇溶液共热制备CH3-CH═CH2 |
B、乙酰水杨酸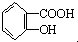 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备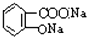 |
| C、向CH3CH2Br中滴入AgNO3溶液以检验溴元素 |
| D、甲苯在溴化铁催化作用下与液溴反应生成2,4,6-三溴甲苯 |
在某容器中,C+H2O(g)?CO+H2反应达到平衡,在温度、体积不变的情况下,向容器中充入一定量H2,当建立新平衡时( )
| A、CO、H2的浓度都比原平衡时的要小 |
| B、CO、H2的浓度都比原平衡时的要大 |
| C、H2、H2O(g)的浓度都比原平衡时的要大 |
| D、CO、H2O(g)的浓度都比原平衡时的要大 |
下列各组离子中,在溶液中能大量共存的是( )
| A、HCO3-、Cl-、Na+、H+ |
| B、Al3+、K+、OH-、SO42- |
| C、Fe2+、NO3-、SO42-、H+ |
| D、K+、Al3+、SO42-、NO3- |
下列说法正确的是( )
| A、一定温度下,当弱酸的浓度相同时,电离常数越大,酸性越强 |
| B、合成氨的反应,正反应的平衡常数和逆反应的平衡常数相同 |
| C、实验测定酸碱滴定曲线时,要保证整个过程测试和记录pH的间隔相同 |
| D、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
 某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如下图.材料1:NH3是强还原剂,能将某些金属氧化物还原为金属单质或低价态的氧化物.如:2NH3+3CuO
某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如下图.材料1:NH3是强还原剂,能将某些金属氧化物还原为金属单质或低价态的氧化物.如:2NH3+3CuO