题目内容
18.已知氢气和氧气反应生成1mol水蒸气时可以放出241.8kJ的热量,1g水蒸气转化为液态水放热2.444kJ.写出表示H2燃烧热的热化学方程式H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol.分析 根据热化学方程式的书写原则写出氢气燃烧生成气态水的热化学方程式,方程中的热量和化学计量数要对应;
氢气的燃烧热是值1mol氢气完全燃烧生成液态水放出的热量,单位是kJ/mol;根据m=nM计算1mol水的质量为18g,进而计算1mol气态水转化成液态水放出的热量,结合氢气与氧气反应生成气态水的反应热计算生成液态水的反应热.
解答 解:氢气和氧气反应生成1mol水蒸气放热241.8kJ,该反应的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8kJ/mol;
1g水蒸气转化成液态水放热2.44kJ,故18g水蒸气转化成液态水放出热量2.444kJ×18=43.992kJ,故反应H2(g)+$\frac{1}{2}$O2(g)═H2O(l)的反应热△H=-(241.8kJ/mol+43.992kJ/mol)=-285.8kJ/mol,故氢气的燃烧热为285.8kJ/mol,燃烧热的热化学方程式;H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol,
故答案为:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol.
点评 本题考查热化学方程式的书写与反应热的计算、燃烧热等,题目难度不大,注意掌握热化学方程式的书写,燃烧热注意把握可燃物为1mol,生成稳定的氧化物.

练习册系列答案
相关题目
4.五种短周期元素在周期表中的相对位置如图所示,其中Q元素最外层电子数是其电子层数的2倍,请用具体的化学用语回答以下问题:
(1)元素Q在周期表中的位置是第三周期VIA族.
(2)W、Q的最高价氧化物对应的含氧酸的酸性:HClO4>H2SO4(用化学式表示,下同)
| X | Y | ||
| Z | Q | W |
(2)W、Q的最高价氧化物对应的含氧酸的酸性:HClO4>H2SO4(用化学式表示,下同)
9.已知在25℃下,101kPa下,1g辛烷C8H18燃烧生成二氧化碳和液态水时放出48.40kJ热量.表示上述反应的热化学方程式正确的是( )
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(g)△H=-48.40kJ•mol-1 | |
| B. | 2C8H18(l)+25O2(g)═16CO2(g)+18H2O(g)△H=+11035.2kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=+5517.6kJ•mol-1 | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-5517.6kJ•mol-1 |
6.在25℃、101kPa时,充分燃烧一定量的甲醇,放出热量Q kJ(Q>0),经测定完全吸收生成的二氧化碳需要消耗5mol•L-1的KOH溶液100mL,恰好生成正盐.则此条件下,下列热化学方程式正确的是( )
| A. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(l)△H=-2Q kJ•mol-1 | |
| B. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(l)△H=-4Q kJ•mol-1 | |
| C. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(l)△H=-Q kJ•mol-1 | |
| D. | CH3OH(l)+2O2(g)═CO2(g)+2H2O(g)△H=-4Q kJ•mol-1 |
3.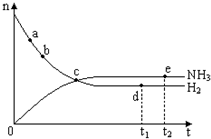 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应),673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )| A. | 点a的正反应速率比点b的大 | |
| B. | 点 c处反应达到平衡 | |
| C. | 点d(t1时刻) 和点e(t2时刻)处n(N2)不一样 | |
| D. | 其他条件不变,573K下反应至t1时刻,n(H2)比图中d点的值大 |
7.下列有关化学用语使用正确的是( )
| A. | 硫离子的结构示意图: | |
| B. | 原子核内有10个中子的氧离子:${\;}_{8}^{18}$O | |
| C. | NH4Cl的电子式: | |
| D. | 乙烯的结构简式C2H4 |
8.下列说法不正确的是( )
| A. | 假说经过反复验证和修正,才发展成为科学的理论 | |
| B. | 研究物质的性质常用观察、实验、分类、比较等方法 | |
| C. | 胶体中分散质微粒能透过滤纸不能透过半透膜 | |
| D. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 |
