题目内容
12.二氧化锰是化学工业中常用的氧化剂和有机合成中的催化剂,其主要制备方法是碳酸锰热分解,反应原理为2MnCO3+O2═2MnO2+2CO2.经研究发现该反应过程为①MnCO3═MnO+CO2 ②2MnO+O2═2MnO2.回答下列问题:
(1)某温度下该平衡体系的压强为P,CO2、O2的物质的量分别为n1和n2,用平衡分压代替平衡浓度,碳酸锰热分解反应的平衡常数K=$\frac{p{{n}_{1}}^{2}}{{n}_{2}({n}_{1}+{n}_{2})}$(分压=总压×物质的量分数);K与反应①、②的平衡常数K1、K2的关系为K=K12×K2.
(2)反应②在低温下能自发进行,则其△H<0(填“>”、“<”或“=”).
分析 (1)生成物浓度的幂之积比上反应浓度的幂之积,固体不代入表达式;2MnCO3+O2═2MnO2+2CO2为方程①②之和,所以K=K1×K2;
(2)反应自发进行的判断依据是△H-T△S<0,反应自发进行,△H-T△S>0,反应非自发进行.
解答 解:(1)反应①的平衡常数表达式K1=$\frac{{c}^{2}(C{O}_{2})}{c({O}_{2})}$=$\frac{(\frac{P{n}_{1}}{{n}_{1}+{n}_{2}})^{2}}{\frac{P{n}_{2}}{{n}_{1}+{n}_{2}}}$=$\frac{p{{n}_{1}}^{2}}{{n}_{2}({n}_{1}+{n}_{2})}$,K与反应①、②的平衡常数K1、K2关系为:2MnCO3+O2═2MnO2+2CO2为方程①的系扩大2倍后与②之和所以K=K12×K2,
故答案为:$\frac{p{{n}_{1}}^{2}}{{n}_{2}({n}_{1}+{n}_{2})}$;K=K12×K2;
(2)反应②在低温下能,只有△H<0,△G<0反应自发,
故答案为:<.
点评 本题考查化学平衡常数的含义,平衡移动、反应方向进行判断等相关知识,题目难度中等,试题综合性强,学生要有一定的化学基本功才能解决,试题培养了学生的灵活应用能力.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
2.在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
回答下列问题:
(1)该反应为吸热反应(填“吸热”或“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是BC(多选扣分).
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(3)850℃时,若向一容积可变的密闭容器中同时充入1.0molCO、3.0molH2O、1.0molCO2和xmolH2,则:
①当x=5.0时,上述平衡向逆反应(填“正反应”、“逆反应”、“恰好平衡”)方向进行.
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是0≤x<3.
(4)在850℃时,若设x=5.0mol和x=6.0mol,其他物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a< b (填“>”、“<”或“=”).
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为吸热反应(填“吸热”或“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是BC(多选扣分).
A.容器中压强不变 B.混合气体中 c(CO)不变
C.υ正(H2)=υ逆(H2O) D.c(CO2)=c(CO)
(3)850℃时,若向一容积可变的密闭容器中同时充入1.0molCO、3.0molH2O、1.0molCO2和xmolH2,则:
①当x=5.0时,上述平衡向逆反应(填“正反应”、“逆反应”、“恰好平衡”)方向进行.
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是0≤x<3.
(4)在850℃时,若设x=5.0mol和x=6.0mol,其他物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a< b (填“>”、“<”或“=”).
3.利用如图所示装置,将10mL CCl4(沸点76.7℃)和10mL甲苯(沸点110.6℃)的混合物进行蒸馏分离.下列说法正确的是( )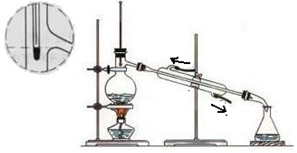

| A. | 冷凝水的进出口方向正确 | B. | 应选用20 mL的蒸馏烧瓶 | ||
| C. | 温度计液泡应插在混合液中 | D. | 锥形瓶中收集到的是甲苯 |
20.下列各原子或离子的电子排布式错误的是( )
| A. | Na+ 1s22s22p63s2 | B. | F 1s22s22p5 | ||
| C. | O2- 1s22s22p6 | D. | Ar 1s22s22p63s23p6 |
7.2009年9月25日,我国成功发射“神舟七号”载人飞船.飞船以铝粉与高氯酸铵的混合物为固体燃料,其中高氯酸铵的反应为:2NH4ClO4═N2↑+Cl2↑+2O2↑+4H2O.下列有关叙述正确的是( )
| A. | 铝粉的作用是点燃时可以置换出氧气 | |
| B. | 在反应中NH4ClO4仅起到氧化剂作用 | |
| C. | 该反应属于分解反应,也属于氧化还原反应 | |
| D. | 上述反应瞬间能产生高温,高温是推动飞船飞行的主要因素 |
17.CPAE是蜂胶的主要活性成分,它由咖啡酸合成,合成过程如下.下列说法不正确的是( )
 +
+ →
→ +H2O.
+H2O.
 +
+ →
→ +H2O.
+H2O.| A. | 1molCPAE和1mol咖啡酸分别与足量的NaOH溶液反应,均最多消耗3molNaOH | |
| B. | 与苯乙醇互为同分异构体的酚类物质共有9种 | |
| C. | FeCl3溶液可区别咖啡酸和CPAE | |
| D. | 咖啡酸可发生聚合反应,并且其分子中含有3种官能团 |
4.Na2O2、Cl2、SO2等均能使品红溶液褪色.下列说法正确的是( )
| A. | Na2O2、Cl2、SO2依次属于电解质、单质、非电解质 | |
| B. | Na2O2、Cl2、SO2的漂白原理相同 | |
| C. | 等物质的量的Cl2和SO2同时通入品红溶液,褪色更快 | |
| D. | 在Na2O2中阴、阳离子所含的电子数目相等 |
1.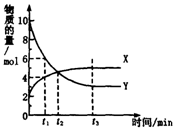 一定温度下在体积为1L的密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在体积为1L的密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在体积为1L的密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在体积为1L的密闭容器内进行着某一反应,X气体、Y气体的物质的量随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为5Y?X | |
| B. | t1时,Y的浓度是X浓度的1.5倍 | |
| C. | 根据t2时的数据,可求出该温度下的平衡常数 | |
| D. | t3时,逆反应速率大于正反应速率 |
10. 钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙.发生反应:
钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙.发生反应:
Ⅰ.WO42ˉ(aq)+Ca(OH)2(s)?CaWO4(s)+2OHˉ(aq) K1
已知:反应Ⅰ的平衡常数K1理论值如下表
请回答下列问题:
(1)判断反应Ⅰ的△S>0、△H>0(填“>”、“=”或“<”),在较高(填“较高”或“较低”)温度下有利于该反应自发进行.
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小.它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s)?Ca2+(aq)+WO42ˉ(aq) K2
Ⅲ.Ca(OH)2(s)?Ca2+(aq)+2OHˉ(aq) K3
①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=K1=$\frac{{K}_{3}}{{K}_{2}}$(用K2、K3表示).
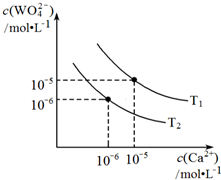
②根据反应Ⅱ,图为不同温度下CaWO4的沉淀溶解平衡曲线.则T1<T2(填“>”“=”或“<”).T1时,向0.5mol•Lˉ1钨酸钠的碱性溶液中,加入适量Ca(OH)2,反应达到平衡后WO42ˉ的转化率为60%,此时溶液中c(Ca2+)=5×10ˉ10mol•Lˉ1.(假设反应前后体积不变)
(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率.反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3.
①在反应混合液中不直接通入CO2,其理由是碱性条件下CO2与Ca2+生成难溶物CaCO3,降低WO42ˉ的转化率;
②用平衡移动原理解释添加酸性物质的理由加入酸性物质与OHˉ反应,使溶液中OHˉ浓度减小,平衡向生成CaWO4的方向移动.
 钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙.发生反应:
钨酸钙是非常重要的化学原料,主要用于生产钨铁、钨丝及钨合金等钨制品.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙.发生反应:Ⅰ.WO42ˉ(aq)+Ca(OH)2(s)?CaWO4(s)+2OHˉ(aq) K1
已知:反应Ⅰ的平衡常数K1理论值如下表
| 温度/℃ | 25 | 50 | 90 | 100 |
| K1 | 79.96 | 208.06 | 222.88 | 258.05 |
(1)判断反应Ⅰ的△S>0、△H>0(填“>”、“=”或“<”),在较高(填“较高”或“较低”)温度下有利于该反应自发进行.
(2)氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,溶解度均随温度升高而减小.它们在水中存在如下沉淀溶解平衡:
Ⅱ.CaWO4(s)?Ca2+(aq)+WO42ˉ(aq) K2
Ⅲ.Ca(OH)2(s)?Ca2+(aq)+2OHˉ(aq) K3
①根据反应Ⅰ~Ⅲ,可推导出K1、K2与K3之间的关系,则K1=K1=$\frac{{K}_{3}}{{K}_{2}}$(用K2、K3表示).
②根据反应Ⅱ,图为不同温度下CaWO4的沉淀溶解平衡曲线.则T1<T2(填“>”“=”或“<”).T1时,向0.5mol•Lˉ1钨酸钠的碱性溶液中,加入适量Ca(OH)2,反应达到平衡后WO42ˉ的转化率为60%,此时溶液中c(Ca2+)=5×10ˉ10mol•Lˉ1.(假设反应前后体积不变)
(3)制取钨酸钙时,适时向反应混合液中添加适量的某种酸性物质,有利于提高WO42ˉ的转化率.反应后过滤,再向滤液中通CO2,进一步处理得到Na2CO3.
①在反应混合液中不直接通入CO2,其理由是碱性条件下CO2与Ca2+生成难溶物CaCO3,降低WO42ˉ的转化率;
②用平衡移动原理解释添加酸性物质的理由加入酸性物质与OHˉ反应,使溶液中OHˉ浓度减小,平衡向生成CaWO4的方向移动.