题目内容
已知0.1mol X2O72- 能将100mL,3mol/L SO32- 氧化成SO42-,则X元素被还原后的化合价是
A.0 B.+2 C.+3 D.+4
C
【解析】
试题分析:亚硫酸根离子中的硫元素化合价从+4升高到+6,总共失去的电子物质的量为2×0.1×3=0.6摩尔,等于X元素得到的电子的物质的量,故X变化的化合价为0.6÷0.1÷2=3,原来X的化合价为+6,故被还原后的化合价为+6-3=+3,故选C。
考点:氧化还原反应中电子守恒。

练习册系列答案
相关题目
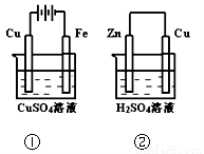
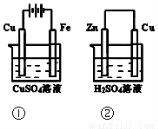 下列叙述正确的是
下列叙述正确的是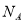 个氢气分子所占的体积为22.4L
个氢气分子所占的体积为22.4L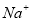 与
与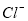 离子总数为
离子总数为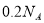
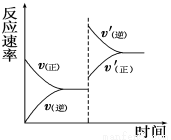
 pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,
pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图所示,