题目内容
在某容积为2L的恒容密闭容器中,有A、B、C、D四种气体发生反应,回答下列问题:

(1)如果四种气体物质的量(n)随时间(t)的变化曲线如图1所示,则:
①该反应的化学方程式为 (反应物与生成物用字母表示,下同),反应的化学平衡常数表达式为 ;
②在2min时,图象发生改变的原因可能是 (用字母表示)
A.升高温度 B.充入A物质增大压强
C.分离出C物质 D.加入催化剂
(2)如果反应方程式为A(g)+B(g)?C(g)+D(g),已知该反应的平衡常数K和温度t的关系如下表所示,A、B的起始浓度均为1mol?L-1,C、D为0mol?L-1
①该反应是 反应(填“吸热”或“放热”),830℃反应达到平衡时,CO的转化率为 .
②已知某温度下,反应以上述的初始浓度开始,到6min时到达化学平衡状态,c(D)随时间t(min)变化的部分曲线如图2所示,平衡后在7min时再充入1mol的D气体,发现反应至9min时各物质浓度不再变化,请在图2中画出从充入D的一刻到10min时D浓度的变化曲线.

(1)如果四种气体物质的量(n)随时间(t)的变化曲线如图1所示,则:
①该反应的化学方程式为
②在2min时,图象发生改变的原因可能是
A.升高温度 B.充入A物质增大压强
C.分离出C物质 D.加入催化剂
(2)如果反应方程式为A(g)+B(g)?C(g)+D(g),已知该反应的平衡常数K和温度t的关系如下表所示,A、B的起始浓度均为1mol?L-1,C、D为0mol?L-1
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
②已知某温度下,反应以上述的初始浓度开始,到6min时到达化学平衡状态,c(D)随时间t(min)变化的部分曲线如图2所示,平衡后在7min时再充入1mol的D气体,发现反应至9min时各物质浓度不再变化,请在图2中画出从充入D的一刻到10min时D浓度的变化曲线.
考点:物质的量或浓度随时间的变化曲线,化学平衡常数的含义,化学平衡的影响因素
专题:化学平衡专题
分析:(1)①根据物质的量的变化判断反应物和生成物,再根据物质的量的变化之比等于化学计量数之比书写方程式;化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值;
②由图象可知2min时反应速率加快,据此分析;
(2)①由表中数据可知,温度越高,平衡常数越小,说明升高温度平衡向逆反应方向移动,据此判断;令参加反应的B的物质的量为x mol,利用三段式表示出平衡时各组分的物质的量,由于反应前后气体的化学计量数之和相等,故利用物质的量代替浓度代入平衡常数列方程计算;
②7min时再充入1mol的D气体,D的物质的量瞬间增大到1mol/L,然后化学平衡向逆反应方向移动,即D浓度减小,根据化学平衡常数计算出到9min时D浓度,画出图象.
②由图象可知2min时反应速率加快,据此分析;
(2)①由表中数据可知,温度越高,平衡常数越小,说明升高温度平衡向逆反应方向移动,据此判断;令参加反应的B的物质的量为x mol,利用三段式表示出平衡时各组分的物质的量,由于反应前后气体的化学计量数之和相等,故利用物质的量代替浓度代入平衡常数列方程计算;
②7min时再充入1mol的D气体,D的物质的量瞬间增大到1mol/L,然后化学平衡向逆反应方向移动,即D浓度减小,根据化学平衡常数计算出到9min时D浓度,画出图象.
解答:
解:(1)达到平衡时A、B、C、D改变的物质的量分别为0.8mol、1.0mol、1.2mol、0.8mol,且A、B的物质的量减少,应为反应物;C、D的物质的量增加,应为生成物,故反应的化学方程式为4A+5B?6C+4D;化学平衡常数为K=
,故答案为:4A+5B?6C+4D;
;
②从图象看,2~3min时图象的斜率变大,说明化学反应速率变快.增大压强、加入催化剂均增大化学反应速率,而降低温度减小化学反应速率.增加A的物质的量,虽能加快化学反应速率,但图象要产生突变,故答案为:AD;
(2)①由表中数据可知,温度越高,平衡常数越小,说明升高温度平衡向逆反应方向移动,升高温度平衡向吸热反应方向移动,故正反应为放热反应;设平衡时参加反应的B的物质的量为xmol/L,则:
A(g)+B(g)?C(g)+D(g)
开始(mol/L):1 1 0 0
变化(mol/L):x x x x
平衡(mol/L):1-x 1-x x x
故
=1,解得x=0.5mol/L,转化率为:
×100%=50%,
故答案为:放热;50%;
②“反应以上述的初始浓度开始”,6min时,D浓度为0.5mol/L,则平衡时,各物质浓度均为0.5mol/L,化学平衡常数为:
=1;7min时再充入1mol的D气体,D的物质的量瞬间增大到1mol/L,然后化学平衡向逆反应方向移动,即D浓度减小;9min时达到平衡状态,平衡时参加反应的D的物质的量为ymol/L,则:
A(g)+B(g)?C(g)+D(g)
开始(mol/L):0.5 0.5 0.5 1
变化(mol/L):y y y y
平衡(mol/L):0.5+y 0.5+y 0.5-y 1-y
=1,y=0.1mol/L,即9min时,D浓度为1mol/L-0.1mol/L=0.9mol/L,根据以上分析画出曲线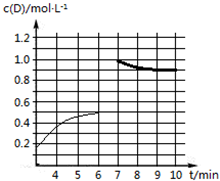 ,
,
故答案为: .
.
| c6(C)?c4(D) |
| c4(A)?c5(B) |
| c6(C)?c6(D) |
| c4(A)?c5(B) |
②从图象看,2~3min时图象的斜率变大,说明化学反应速率变快.增大压强、加入催化剂均增大化学反应速率,而降低温度减小化学反应速率.增加A的物质的量,虽能加快化学反应速率,但图象要产生突变,故答案为:AD;
(2)①由表中数据可知,温度越高,平衡常数越小,说明升高温度平衡向逆反应方向移动,升高温度平衡向吸热反应方向移动,故正反应为放热反应;设平衡时参加反应的B的物质的量为xmol/L,则:
A(g)+B(g)?C(g)+D(g)
开始(mol/L):1 1 0 0
变化(mol/L):x x x x
平衡(mol/L):1-x 1-x x x
故
| x2 |
| (1-x)2 |
| 0.5mol/L |
| 1mol/L |
故答案为:放热;50%;
②“反应以上述的初始浓度开始”,6min时,D浓度为0.5mol/L,则平衡时,各物质浓度均为0.5mol/L,化学平衡常数为:
| (0.5mol/L)2 |
| (0.5mol/L)2 |
A(g)+B(g)?C(g)+D(g)
开始(mol/L):0.5 0.5 0.5 1
变化(mol/L):y y y y
平衡(mol/L):0.5+y 0.5+y 0.5-y 1-y
| (0.5-y)?(1-y) |
| (0.5+y)2 |
 ,
,故答案为:
 .
.
点评:本题考查学生对图象的观察分析能力,图象中各物质在不同的时间段中物质的量的变化趋势是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100kPa时,1mol金刚石和1mol石墨在氧气中完全燃烧放出的热量分别为393.5kJ和395.4kJ,下列说法不正确的是( )
| A、1mol石墨转化为1 mol金刚石时要吸收1.9 kJ的热能 |
| B、1mol石墨比1 mol金刚石的能量低 |
| C、1mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ |
| D、石墨比金刚石稳定 |
Na2SO4和Al2(SO4)3的混合溶液中,Al3+的浓度为0.2mol/L,SO42-的浓度为0.4mol/L,溶液中Na+的物质的量浓度是( )
| A、0.1mol/L |
| B、0.2mol/L |
| C、0.3mol/L |
| D、0.4mol/L |
 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题: