题目内容
(11分)2013年雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g) 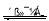 2CO2 (g) +N2 (g) 在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
2CO2 (g) +N2 (g) 在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
 据此判断:
据此判断:
①该反应的平衡常数表达式为 。
②该反应的ΔH 0(选填“>”、“<”)。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在右
图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) 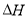 =-867kJ·mol-1
=-867kJ·mol-1
2NO2(g)  N2O4(g)
N2O4(g) 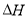 =-56.9kJ·mol-1
=-56.9kJ·mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式 。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过光电转化原理以廉价原料制备新产品的示意图。
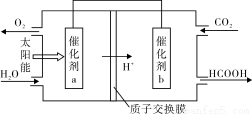
写出上述光电转化过程的化学反应方程式 。催化剂a、b之间连接导线上电子流动方向是 (填a→b或b→a)。
(1)① ②<
②<
③
(2)①CH4(g)+N2O4(g) = N2(g)+CO2(g)+2H2O(g)  =-810.1 kJ·mol-1
=-810.1 kJ·mol-1
②2CO2+2H2O 光照 2HCOOH+O2 a→b
【解析】
试题解析:(1)①化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,故答案为: ;②图象中T1先达平衡,即T1>T2,由于T1中c(CO2)较小,即温度升高,化学平衡向逆反应方向移动,为放热反应,故答案为:<;③催化剂的表面积S1>S2,S2反应速率比S1小,即达到平衡所需时间长,由于催化剂不影响化学平衡的移动,达平衡状态时,与T2、S1条件下相同,故答案为:
;②图象中T1先达平衡,即T1>T2,由于T1中c(CO2)较小,即温度升高,化学平衡向逆反应方向移动,为放热反应,故答案为:<;③催化剂的表面积S1>S2,S2反应速率比S1小,即达到平衡所需时间长,由于催化剂不影响化学平衡的移动,达平衡状态时,与T2、S1条件下相同,故答案为:
 ;
;
(2)①第一个反应减第二个反应就可得:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=-810.1 kJ
?mol-1;②体系中进入的物质为:CO2和H2O,则反应物为:CO2和H2O,得到的物质为:HCOOH和O2,生成物为:HCOOH和O2,利用氧化还原方程式的配平写出化学方程式为:2CO2+2H2O光照2HCOOH+O2 ;体系中氢离子从 a→b,则电流的方向为:b→a,电子的流向为:a→b。
考点:化学平衡;热化学方程式;电化学

 步步高达标卷系列答案
步步高达标卷系列答案下表是3种物质的溶解度(20 ℃),下列说法中正确的是
物质 | MgCl2 | Mg(OH)2 | MgCO3 |
溶解度(g/100 g) | 74 | 0.000 84 | 0.01 |
A.已知MgCO3的Ksp=6.82×10-6 mol2·L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)·c(CO32-)=6.82×10-6 mol2·L-2
B.除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液
C.将表中三种物质与水混合,加热、灼烧,最终的固体产物相同
D.用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O

 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O


 H+ + H2PO3-。亚磷酸与足量NaOH溶液反应,生和Na2HPO3。
H+ + H2PO3-。亚磷酸与足量NaOH溶液反应,生和Na2HPO3。