题目内容
14.(1)由金红石(TiO2)制取单质Ti,涉及到的步骤为:TiO2→TiCl4$\stackrel{镁/800℃/Ar}{→}$Ti已知:①C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol?1
②2CO(g)+O2(g)═2CO2(g);△H=-566kJ•mol?1
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g);△H=+141kJ•mol?1
则TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g)的△H=-80kJ/mol
(2)P4(s,白磷)+5O2(g)═P4O10(s)△H1=-2983.2kJ/molP(s,红磷)+$\frac{5}{4}{O_2}(g)=\frac{1}{4}{P_4}{O_{10}}$(s)△H2=-738.5kJ/mol,则白磷转化为红磷的热化学方程式P4(s,白磷)=4P(s,红磷)△H=-29.2kJ/mol.相同的状况下,能量较低的是红磷;白磷的稳定性比红磷低(填“高”或“低”).
(3)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示:

①A中反应的离子方程式为Fe+2H+=Fe2++H2↑.
②B中Sn极作正极,C中被腐蚀的金属是锌.
分析 (1)根据盖斯定律将三个化学方程式进行相加减得到TiO2(s)+2Cl2(g)+2C(s)═TiCl4(s)+2CO(g),反应热也相应的相加减计算得到;
(2)根据盖斯定律可以计算化学反应的焓变,进而书写热化学方程式;根据物质的总能量与反应热的关系判断,能量越高物质越稳定;
(3)①铁与稀硫酸反应生成硫酸亚铁和氢气;
②活泼性强的为负极,活泼性弱的为正极,负极被腐蚀.
解答 解:(1)已知:①C(s)+O2(g)═CO2(g);△H=-393.5kJ•mol-1
②2CO(g)+O2(g)═2CO2(g);△H=-566kJ•mol-1
③TiO2(s)+2Cl2(g)═TiCl4(s)+O2(g);△H=+141kJ•mol-1
根据盖斯定律①×2-②+③得
TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=(-393.5kJ•mol-1)×2-(-566kJ•mol-1)+(+141kJ•mol-1),
即TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)△H=-80kJ/mol,
故答案为:-80kJ/mol;
(2)P4(s,白磷)+5O2(g)=P4O10(s)△H1=-2983.2kJ/mol…①
P(s,红磷)+$\frac{5}{4}$O2(g)=$\frac{1}{4}$P4O10(s)△H2=-738.5kJ/mol,…②
根据盖斯定律:①-②×4可得:P4(s,白磷)=4P(s,红磷)△H=(-2983.2kJ/mol)-(-738.5kJ)×4=-29.2kJ/mol,
说明白磷转化为红磷是放热反应,相同的状况下,红磷能量比白磷低,而能量越低,物质越稳定,故白磷不如红磷稳定,
故答案为:P4(s,白磷)=4P(s,红磷)△H=-29.2kJ/mol;红磷;低;
(3)①铁与硫酸反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑,离子方程式为:Fe+2H+=Fe2++H2↑;
故答案为:Fe+2H+=Fe2++H2↑;
②B中铁比锡活泼,锡为原电池正极,C中锌为负极,铁为正极,锌被腐蚀;
故答案为:正;锌.
点评 本题考查了热化学方程式的书写、盖斯定律的应用、金属的电化学腐蚀与防护,题目难度不大,注意金属的电化学腐蚀与化学腐蚀的区别以及盖斯定律的含义和应用方法.

| A. | 1mol铁与足量的氯气完全反应转移的电子数为2NA | |
| B. | 常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA | |
| C. | 标准状况下,1molCO2、CO的混合气中含有的碳原子数为NA | |
| D. | 1L1mol•L-1CuCl2溶液中含有的氯离子数为NA |
| A. | 滴加KSCN溶液 | B. | 先加硝酸根,再加硝酸酸化 | ||
| C. | 利用焰色反应 | D. | 先加盐酸酸化,再加氯化钡 |
 硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.
硫酸生产主要有硫磺法和硫铁矿法等,这两种制法均经过催化氧化步骤.(1)钒触媒(V2O5)能加快SO2的氧化速率,V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理的化学方程式SO2+V2O5═SO3+2VO2,4VO2+O2═2V2O5.
(2)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1.
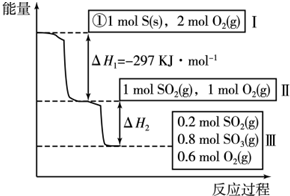
恒温条件下,容积为1L的恒容容器中,硫可以发生如下转化,其反应过程和能量关系如图所示.
①写出能表示硫的燃烧热的热化学方程式为S(s)+O2(g)=SO2(g)△H=-297kJ•mol-1.
②在相同条件下,充入1molSO3和0.5mol的O2则达到平衡时SO3的转化率为20%,此时该反应吸收19.66kJ的能量.
(3)在温度相同、体积均为1L的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下.
已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1.
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol SO2、1mol O2 | 2mol SO3 | 4mol SO2、2mol O2、 |
| 平衡时n(SO3) | 1.6mol | n2 | n3 |
| 能量变化 | 放出a kJ | 吸收b kJ | 放出c kJ |
| SO2或SO3的转化率 | α1 | α2 | α3 |
②计算在该温度下此反应的平衡常数为80.
 二甲醚又称甲醚,简称DME,熔点-141.5℃,沸点-24.9℃,与石油液化气(LPG)相似,被誉为“21世纪的清洁燃料”.制备原理如下:
二甲醚又称甲醚,简称DME,熔点-141.5℃,沸点-24.9℃,与石油液化气(LPG)相似,被誉为“21世纪的清洁燃料”.制备原理如下:I.由天然气催化制备二甲醚:
①2CH4(g)+O2(g)?CH3OCH3(g)+H2O(g)△H1
II.由合成气制备二甲醚:
②CO(g)+2H2(g)?CH3OH(g)△H2=-90.7kJ•mol-1
③2CH3OH(g)?CH3OCH3(g)+H2O(g)△H3
回答下列问题:
(1)若甲烷和二甲醚的燃烧热分别是890.3kJ•mol-1、1453.0kJ•mol-1;1mol液态水变为气态水要吸收44.0kJ的热量.反应③中的相关的化学键键能数据如表:
| 化学键 | H-H | C-O | H-O(水) | H-O(醇) | C-H |
| E/(kJ.mol-1) | 436 | 343 | 465 | 453 | 413 |
(2)反应①的化学平衡常数表达式为$\frac{c(C{H}_{3}OC{H}_{3})•c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$.
制备原理I中,在恒温、恒容的密闭容器中合成,将气体按n(CH4):n(O2)=2:1混合,能正确反映反应①中CH4的体积分数随温度变化的曲线是b.
下列能表明反应①达到化学平衡状态的是bd.
a.混合气体的密度不变
b.反应容器中二甲醚的百分含量不变
c.反应物的反应速率与生成物的反应速率之比等于化学计量数之比
d.混合气体的压强不变
(3)有人模拟制备原理II,在500K时的2L的密闭容器中充入2molCO和6molH2,8min达到平衡,平衡使CO的转化率为80%,c(CH3OCH3)=0.3mol•L-1,用H2表示反应②的速率是0.2mol/(L•min);可逆反应③的平衡常数K3=2.25.
若在500K时,测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v(正)>v(逆),说明原因浓度商Q=$\frac{c(C{H}_{3}OC{H}_{3})•c({H}_{2}O)}{{c}^{2}(C{H}_{3}OH)}$=$\frac{x•x}{{x}^{2}}$=1<2.25,反应正向进行,v(正)>v(逆).
| A. | Ba2+、Na+、NO3-、SO42- | B. | Mg2+、NH4+、NO3-、SO42- | ||
| C. | NH4+、K+、Cl-、OH- | D. | K+、H+、SO32-、ClO- |
| A. | 苯中含有三个碳碳双键 | |
| B. | 乙酸中的官能团是羟基 | |
| C. | 乙醇不能与金属钠反应 | |
| D. | 海水淡化的方法主要有:蒸馏法、电渗析法、离子交换法等 |
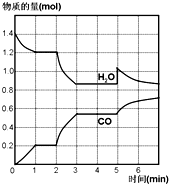 在一容积为2L的密闭容器中,高温下发生下列反应:C(s)+H2O(g)?CO(g)+H2(g),其中H2O、CO的物质的量(mol)随时间(min)的变化曲线如图所示:
在一容积为2L的密闭容器中,高温下发生下列反应:C(s)+H2O(g)?CO(g)+H2(g),其中H2O、CO的物质的量(mol)随时间(min)的变化曲线如图所示: