题目内容
某无色溶液中含有:①K+、②Ba2+、③Cl-、④Br-、⑤SO32-、⑥CO32-、⑦SO42-中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:下列结论正确的是( )
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| ③ | 向②所得溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A、可能含有的离子是①②⑦ |
| B、肯定含有的离子是①④ |
| C、不能确定的离子是①③⑦ |
| D、肯定没有的离子是②⑤⑥ |
考点:常见阴离子的检验,常见阳离子的检验
专题:
分析:①用pH试纸检验溶液的pH大于7,说明溶液呈碱性,应含有弱酸的酸根离子;
②向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙色,说明溶液中含有Br-;
③向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生,该沉淀为BaSO4,但不能确定是否含有SO42-,因SO32-可被硝酸氧化生成SO42-;
④过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生,该沉淀为AgCl,但不能确定溶液中是否含有Cl-,因所加氯水中含有Cl-.
②向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙色,说明溶液中含有Br-;
③向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生,该沉淀为BaSO4,但不能确定是否含有SO42-,因SO32-可被硝酸氧化生成SO42-;
④过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生,该沉淀为AgCl,但不能确定溶液中是否含有Cl-,因所加氯水中含有Cl-.
解答:
解:①用pH试纸检验溶液的pH大于7,说明溶液呈碱性,应含有弱酸的酸根离子,该离子可能为SO32-或CO32-,则溶液中一定不存在Ba2+,因二者分别能与钡离子生成沉淀而不能大量共存,
一定含有K+,根据溶液呈电中性原则,阳离子只有K+;
②向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙色,说明溶液中含有Br-;
③向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生,该沉淀为BaSO4,但不能确定是否含有SO42-,因SO32-可被硝酸氧化生成SO42-;
④过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生,该沉淀为AgCl,但不能确定溶液中是否含有Cl-,因所加氯水中含有Cl-.
由以上分析可知,溶液中一定含有的离子为①④,可能含有的离子为③⑤⑥(⑤⑥至少含有1种),一定不存在的是②,故选:B.
一定含有K+,根据溶液呈电中性原则,阳离子只有K+;
②向溶液中滴加氯水,再加入CCl4振荡,静置CCl4层呈橙色,说明溶液中含有Br-;
③向所得水溶液中加入Ba(NO3)2溶液和稀HNO3有白色沉淀产生,该沉淀为BaSO4,但不能确定是否含有SO42-,因SO32-可被硝酸氧化生成SO42-;
④过滤,向滤液中加入AgNO3溶液和稀HNO3有白色沉淀产生,该沉淀为AgCl,但不能确定溶液中是否含有Cl-,因所加氯水中含有Cl-.
由以上分析可知,溶液中一定含有的离子为①④,可能含有的离子为③⑤⑥(⑤⑥至少含有1种),一定不存在的是②,故选:B.
点评:本题考查离子反应及离子组成分的判断,题目难度不大,本题注意把握离子的性质及离子共存问题.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
已知2H2(g)+O2(g)→2H2O(g)+483.6kJ.下列说法或表达正确的是( )
| A、在相同的条件下,2mol 氢气与 1 mol 氧气的总能量小于2mol 水蒸气的总能量 | ||
B、H2(g)+
| ||
| C、氢气燃烧是放热反应,所以氢气和氧气反应不需要其他外界条件即可发生 | ||
| D、任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
下列说法中正确的是( )
| A、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
| B、需要加热的化学反应,生成物的总能量一定高于反应物的总能量 |
| C、熵减的反应一定是非自发反应 |
| D、己知2C(s)+2O2(g)=2CO2(g)△H1,2C(s)+O2(g)=2CO(g)△H2,则△H1<△H2 |
下列元素一定为主族元素的是( )
| A、其原子最外电子层只1个电子的元素 |
| B、最低负化合价为-3价的元素 |
| C、其原子最外层电子数大于电子层数的元素 |
| D、最高价氧化物对应的水化物是酸的元素 |
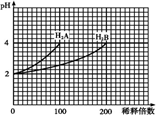 常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述不正确的是( )
常温下,取pH=2的两种二元酸H2A与H2B各1mL,分别加水稀释,测得pH变化与加水稀释倍数有如图所示变化,则下列有关叙述不正确的是( )| A、H2A为二元强酸 |
| B、pH=4的NaHA水溶液中离子浓度大小为:c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-) |
| C、含NaHA、NaHB的混合溶液中,离子浓度大小为:c(Na+)=c(A2-)+c(HB-)+c(B2-)+c(H2B) |
| D、Na2B的水溶液中,离子浓度大小为:c(Na+)>c(B2-)>c(OH-)>c(H+) |
 在一个体积为2L的真空密闭容器中加入0.5molCaCO3,发生反应CaCO3(s)═CaO (s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线.请按要求回答下列问题:
在一个体积为2L的真空密闭容器中加入0.5molCaCO3,发生反应CaCO3(s)═CaO (s)+CO2(g),测得二氧化碳的物质的量浓度随温度的变化关系如图表示,图中A表示CO2的平衡浓度与温度的关系曲线,B表示不同温度下反应经过相同时间时CO2的物质的量浓度的变化曲线.请按要求回答下列问题: