题目内容
在一盛有饱和Na2CO3溶液的烧杯中插入惰性电极,保持温度不变,通电一段时间后( )
| A、溶液的PH值增大;碳酸钠溶液的水解程度减小 |
| B、Na+和CO32-的浓度都减小 |
| C、阴极与阳极析出的气体物质的量之比为1:2 |
| D、溶液的浓度不变,有晶体析出 |
考点:电解原理
专题:电化学专题
分析:盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电时氢离子放电生成氢气,氢氧根离子放电生成氧气,即电解水,结合饱和溶液溶剂减少来解答.
解答:
解:盛有饱和碳酸钠溶液的烧杯中插入惰性电极,保持温度不变,通电时氢离子放电生成氢气,氢氧根离子放电生成氧气,即电解水,
A.因温度不变,溶剂减少后还是饱和溶液,则浓度不变,pH不变,故A错误;
B.因温度不变,溶剂减少有晶体析出,溶液Na+和CO32-的浓度不变,故B错误;
C.如阴极产生2mol的氢气与阳极析出的1mol的氧气物质的量之比为2:1,故C错误;
D.因温度不变,溶剂减少后有晶体析出,还是饱和溶液,则溶液浓度不变,故D正确;
故选D.
A.因温度不变,溶剂减少后还是饱和溶液,则浓度不变,pH不变,故A错误;
B.因温度不变,溶剂减少有晶体析出,溶液Na+和CO32-的浓度不变,故B错误;
C.如阴极产生2mol的氢气与阳极析出的1mol的氧气物质的量之比为2:1,故C错误;
D.因温度不变,溶剂减少后有晶体析出,还是饱和溶液,则溶液浓度不变,故D正确;
故选D.
点评:本题考查了电解及饱和溶液的浓度,注意电解水相当于饱和溶液的蒸发,明确温度不变,饱和溶液的浓度不变是解答本题的关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在一定条件下,2体积气体X完全分解生成1体积A2和3体积气体B2,(体积在相同条件下测定),则X的化学式是( )
| A、AB |
| B、AB2 |
| C、AB3 |
| D、A2B3 |
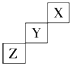 短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法中正确的是( )
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法中正确的是( )| A、Z可能是活泼金属元素 |
| B、X的最高价氧化物对应的水化物是一种强酸 |
| C、Y元素原子的最外层电子数为7 |
| D、Z的最高价氧化物对应水化物的化学式为HZO3 |
NA代表阿伏加德罗常数.下列有关叙述正确的是( )
| A、标准状况下,2.24L H2O含有的分子数等于0.1NA |
| B、常温下,100 mL 1mol/L Na2CO3溶液中钠离子总数为0.1NA |
| C、分子数为NA的CO、N2混合气体体积约为22.4L,质量为28g |
| D、24g O2分子和24g O3分子所含的氧原子数目相等 |
下列图示与对应的叙述相符的是( )
A、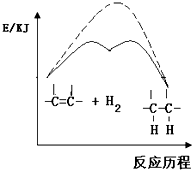 说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下表示 |
B、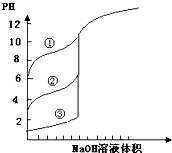 用0.1000mol/L NaOH溶液分别滴定浓度相同的三种一元酸,曲线可确定①的酸性最强 |
C、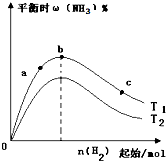 表示合成氨反应在其他条件不变的情况下,改变起始n(H2)对平衡的影响.由此可知,N2转化率最高的是b点;且T1>T2,K2>K1(T1和T2 表示温度,K1、K2表示对应温度下的平衡常数) |
D、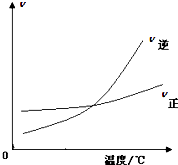 表示可逆反应“A2(g)+3B2 (g)?2AB3(g)”△H小于0 |