��Ŀ����
7���������ƣ�Na2O2������ѧ�������ʣ������Ĺ������ﻹ�����������ƣ�CaO2������֪������������CO2��Ӧ���������ɣ�����S02ͨ��������Ʒ�ĩ��Ҳ���������ɣ��������CO2��SO2��������Ƶķ�Ӧԭ����ͬ����Ҳ�������S02���н�ǿ�Ļ�ԭ�ԣ�CO2��ǿ��ԭ�ԣ���Ӧԭ������ͬ���ݴ��������ʵ����������жϣ�ʵ��һ����һ�����Ĺ������ƹ�����ͨ��������SO2��ȡ��Ӧ��Ĺ������ʵ��̽������֤������������SO2��Ӧ���ص㣮
��1��������裺����1����Ӧ�������ֻ��Na2SO3��֤��SO2δ��������
����2����Ӧ�������ֻ��Na2SO4��֤��SO2��ȫ��������
����3����Ӧ���������Na2SO3��Na2SO4��֤��SO2������������
��ʵ��̽����ʵ�����ͨ���������������жϷ����Ļ�ѧ��Ӧ��ʵ��װ�����£�
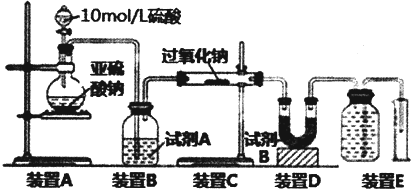
��2���Լ�A����ѡ��Ũ���ᣬ�Լ�B������������δ��Ӧ��SO2��
��3��ʵ����װ��C�й�����������������m1g��װ��D����������m2g��װ��E���ռ���������ΪVL���ѻ���ɱ�״���£����������йز��������жϣ���SO2δ����������V��m1��m2��ϵʽΪV=$\frac{7{m}_{1}}{30}$����SO2��ȫ����������V��m1��m2��ϵʽΪV=0��
��4����SO2��ȫ��������д����Ӧ�Ļ�ѧ����ʽ��Na2O2+SO2=Na2SO4��
���� ��1��SO2δ������ʱ������Na2SO3����SO2��������������Na2SO4��
��2��װ��A�Ʊ�������������������ˮ��Ӧ��װ��A���Լ�������ˮ�����������Լ�ΪŨ���ᣬ���������ȥˮ�������Լ�B��ȥ�����Ķ�����������Ӱ����������ⶨ��
��3����SO2δ��������������Ӧ��2Na2O2+2SO2=2Na2SO3+O2�����C�����ء�E���ռ���������������ò��������㣻
��SO2ȫ���������������ķ�ӦΪ��Na2O2+SO2=Na2SO4����Ӧ���������������ɣ�
��4����SO2��ȫ���������ɹ����������ƣ�
��� �⣺��1����SO2δ������ʱ������Na2SO3����SO2��������������Na2SO4����
����1����Ӧ�����ֻ�� Na2SO3��֤��SO2δ��������
����2����Ӧ�������ֻ�� Na2SO4��֤��SO2��ȫ��������
����3������ΪNa2SO3��Na2SO4�Ļ���֤��SO2������������
�ʴ�Ϊ��Na2SO4��Na2SO3��Na2SO4��
��2���������ƺ�ˮ��Ӧ��װ��A���Լ�������ˮ�����������Լ�ΪŨ���ᣬ���������ȥˮ������װ��EΪ�ⶨ�����������������Ҫ��ʣ��Ķ��������ȥ��ʵ��Bװ������������δ��Ӧ��SO2������Ӱ����������ⶨ��
�ʴ�Ϊ��Ũ�������δ��Ӧ��SO2��
��3����SO2���������
2Na2O2+2SO2=2Na2SO3+O2 �����������ء�m
22.4L 128g-32g=96g
VL m1g
����22.4L��VL=96g��m1g�����V=$\frac{7{m}_{1}}{30}$��
��SO2ȫ���������������ķ�ӦΪ��Na2O2+SO2=Na2SO4����Ӧ���������������ɣ���V=0��
�ʴ�Ϊ��$\frac{7{m}_{1}}{30}$��0��
��4����SO2ȫ���������������ķ�ӦΪ��Na2O2+SO2=Na2SO4��
�ʴ�Ϊ��Na2O2+SO2=Na2SO4��
���� ���⿼������̽��ʵ�飬ʵ�鶨����ʵ�飬�ؼ��Ǹ���װ����ȷʵ��ԭ����������������ѧ����Ϣ��ȡ������������������ѧʵ���������Ѷ��еȣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д� ��ҵ����CO��H2����ȼ�ϼ״���һ���������ܱ������з�����Ӧ���������������ͼ��ʾ����Ӧ����������̬��������˵��������ǣ�������
��ҵ����CO��H2����ȼ�ϼ״���һ���������ܱ������з�����Ӧ���������������ͼ��ʾ����Ӧ����������̬��������˵��������ǣ�������| A�� | ��Ӧ�Ļ�ѧ����ʽ��CO+2H2?CH3OH | |
| B�� | ��Ӧ������3����ʱ�������淴Ӧ������� | |
| C�� | ��Ӧ��10���ӣ�?��CO��=0.075 mol/L•min | |
| D�� | ����ѹǿ��ƽ�������ƶ���K���� |
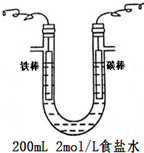 ������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ�����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����Ƶ���650���¹�����ȼ�ϵ�أ���֪���ط�Ӧ�൱��CO��ȼ�գ��Ҹ�����ӦʽΪ2CO+2CO32--4e-=4CO2
������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ�����Li2CO3��Na2CO3�������λ����������ʣ�COΪ����ȼ����������CO2�Ļ����Ϊ������ȼ�����Ƶ���650���¹�����ȼ�ϵ�أ���֪���ط�Ӧ�൱��CO��ȼ�գ��Ҹ�����ӦʽΪ2CO+2CO32--4e-=4CO2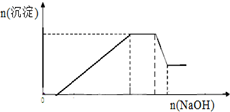 ��֪ij����Һ��Ag+��Fe2+��Al3+��K+��Ba2+��NH4+��NO3-��SO42-�е�������������ɣ���������ʵ�飺[��֪����Al3+��Һ�м�����������Һ������Al��OH��3������������������Һ�����������ܽ⣬��Ӧ����ʽ��Al��OH��3+NaOH=NaAlO2+2H2O]
��֪ij����Һ��Ag+��Fe2+��Al3+��K+��Ba2+��NH4+��NO3-��SO42-�е�������������ɣ���������ʵ�飺[��֪����Al3+��Һ�м�����������Һ������Al��OH��3������������������Һ�����������ܽ⣬��Ӧ����ʽ��Al��OH��3+NaOH=NaAlO2+2H2O]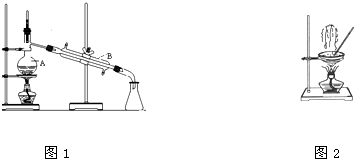 ��1����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺
��1����ͼ����ѧ��ѧ�г����ڻ����ķ�����ᴿ��װ�ã������װ�ûش����⣺ ������A��C4H10O����һ���л��ܼ���A���Է������±仯��
������A��C4H10O����һ���л��ܼ���A���Է������±仯��