题目内容
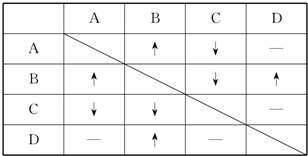
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g),所得实验数据如下表:下列说法正确的是( )
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
| A、实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol?L-1?min-1 |
| B、实验②中,该反应的平衡常数K=2.0 |
| C、实验③中,达到平衡时,X的转化率为40% |
| D、实验④中,达到平衡时,b<0.060 |
考点:化学平衡的计算
专题:
分析:A、根据v=
计算v(M),在利用速率之比等于化学计量数之比计算v(N);
B、由表中数据,利用三段式计算平衡时其它组分的物质的量,由于反应中气体的化学计量数相等,可以用物质的量代替浓度代入平衡常数表达式计算;
C、温度不变平衡常数不变,根据平衡常数可求出转化量,进而求出转化率;
D、对比实验①②的平衡常数可知,正反应为放热反应,升温平衡左移,平衡常数减小,转化率减小,根据实验③中X的转化率为60%,则实验④中X的转化率小于60%,达到平衡时,b<0.060.
| △c |
| △t |
B、由表中数据,利用三段式计算平衡时其它组分的物质的量,由于反应中气体的化学计量数相等,可以用物质的量代替浓度代入平衡常数表达式计算;
C、温度不变平衡常数不变,根据平衡常数可求出转化量,进而求出转化率;
D、对比实验①②的平衡常数可知,正反应为放热反应,升温平衡左移,平衡常数减小,转化率减小,根据实验③中X的转化率为60%,则实验④中X的转化率小于60%,达到平衡时,b<0.060.
解答:
解:A.v(N)=v(M)=
=
=1.0×10-3mol/(L?min),故A错误;
B. X(g)+Y(g)?M(g)+N(g)
起始浓度(mol/L) 0.01 0.04 0 0
转化浓度(mol/L) 0.008 0.008 0.008 0.008
平衡浓度(mol/L) 0.002 0.032 0.008 0.008
实验②中,该反应的平衡常数K=
=
=1.0,故B错误;
C. X(g)+Y(g)?M(g)+N(g)
起始浓度(mol/L) 0.02 0.03 0 0
转化浓度(mol/L) 0.1a 0.1a 0.1a 0.1a
平衡浓度(mol/L)0.02-0.1a 0.03-0.1a 0.1a 0.1a
该反应的平衡常数K=
=
=1.0,解得a=0.12,实验③中,X的转化率=
100%=60%,故C错误;
D.根据三段式可求得,700℃时,化学平衡常数K≈2.6,升高温度至800℃得平衡常数为K=1.0,K减小,即平衡逆向移动,则正反应为放热反应,若④的温度为800℃,恒容体系中,气体体积不变的反应,④与③为等效平衡,b=
a=0.06mol,但④的实际温度为900℃,相比较800℃,平衡逆向移动,b<0.06,故D正确.
故选D.
| △c |
| △t |
| ||
| 5min |
B. X(g)+Y(g)?M(g)+N(g)
起始浓度(mol/L) 0.01 0.04 0 0
转化浓度(mol/L) 0.008 0.008 0.008 0.008
平衡浓度(mol/L) 0.002 0.032 0.008 0.008
实验②中,该反应的平衡常数K=
| c(M)c(N) |
| c(X)c(Y) |
| 0.008×0.008 |
| 0.002×0.002 |
C. X(g)+Y(g)?M(g)+N(g)
起始浓度(mol/L) 0.02 0.03 0 0
转化浓度(mol/L) 0.1a 0.1a 0.1a 0.1a
平衡浓度(mol/L)0.02-0.1a 0.03-0.1a 0.1a 0.1a
该反应的平衡常数K=
| c(M)c(N) |
| c(X)c(Y) |
| 0.1a×0.1a |
| (0.02-0.1a)×(0.03-0.1a) |
| 0.12 |
| 0.2 |
D.根据三段式可求得,700℃时,化学平衡常数K≈2.6,升高温度至800℃得平衡常数为K=1.0,K减小,即平衡逆向移动,则正反应为放热反应,若④的温度为800℃,恒容体系中,气体体积不变的反应,④与③为等效平衡,b=
| 1 |
| 2 |
故选D.
点评:本题考查化学反应速率、化学平衡常数、化学平衡的影响因素等,难度中等.

练习册系列答案
相关题目
下列分子中含有手性碳原子的是( )
| A、CF2Cl2 |
| B、CH3CH2OH |
C、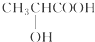 |
| D、CH2═CH-COOH |
将1L含有0.4molCuSO4和0.2molNaCl的水溶液用惰性电极电解,电解一段时间后,在一个电极上增重19.2g,另一个电极上产生气体(标况)的体积是( )
| A、4.48L |
| B、5.6L |
| C、6.72L |
| D、13.44L |
0.1mol/LK2CO3溶液中,由于CO32-的水解,使得c(CO32-)<0.1mol/L.如果要使c(CO32-)更接近于0.1mol/L,可以采取的措施是( )
| A、加入少量盐酸 |
| B、加入适量水 |
| C、加入适当KOH |
| D、加热 |
25℃时,0.1mol/L稀醋酸加水稀释,如图中的纵坐标y可以是( )
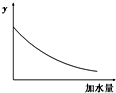

| A、溶液的pH |
| B、醋酸的电离平衡常数 |
| C、醋酸的电离程度 |
| D、溶液的导电能力 |
某合作学习小组讨论辨析以下说法:
①粗盐和酸雨都是混合物;
②纯碱和熟石灰都是碱;
③冰和干冰既是纯净物又是化合物;
④不锈钢和目前流通的硬币都是合金;
⑤盐酸和食醋既是化合物又是酸;
⑥N2O4是酸性氧化物,但不是酸酐;
⑦豆浆和雾都是胶体;
⑧
C、
C、
C是不同种核素.
上述说法不正确的是( )
①粗盐和酸雨都是混合物;
②纯碱和熟石灰都是碱;
③冰和干冰既是纯净物又是化合物;
④不锈钢和目前流通的硬币都是合金;
⑤盐酸和食醋既是化合物又是酸;
⑥N2O4是酸性氧化物,但不是酸酐;
⑦豆浆和雾都是胶体;
⑧
12 6 |
13 6 |
14 6 |
上述说法不正确的是( )
| A、①②③④ | B、①②⑦⑧ |
| C、②③④⑦ | D、②⑤⑥⑧ |
短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13,X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素.下列说法正确的是( )
| A、由X与Y组成的化合物的沸点总低于由X与Z组成的化合物的沸点 |
| B、元素Z、W 的简单离子的电子层结构不同 |
| C、元素Y 的简单气态氢化物的热稳定性比Z 的强 |
| D、只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
用NA表示阿伏伽德罗常数,以下说法正确的是( )
| A、1 mol乙烷中的氢原子被氯原子完全取代,需要氯气分子数为 4 NA |
| B、1 mol的NO2 与水完全反应转移电子数为NA |
| C、在标准状况下2.24 L O2 和3.2 g O3含有氧原子都为0.2 NA. |
| D、在标准状况下2.24 L丙烷和戊烷混合物含分子个数为0.1 NA. |