题目内容
12.为确定某铝热剂(含氧化铁Fe2O3和铝)的组成,分别进行下列实验.(1)取a g样品,向其中加入足量的NaOH溶液,测得生成的气体体积为6.72L(标准状况).则该样品中铝的质量是5.4g.
(2)另取a g样品将其加热引燃发生反应2AI+Fe2O3$\frac{\underline{\;高温\;}}{\;}$AI2O3+2Fe,若恰好完全反应,则a为21.4g,该反应中AI2O3是氧化产物(填“还原产物”或“氧化产物”).
(3)待(2)中反应产物冷却后,加入足量盐酸,反应的离子方程式为Fe+2H+=Fe2++H2↑、Al2O3+6H+=2Al3++3H2O.
分析 (1)铝热剂是金属铝和氧化铁的混合物,金属铝可以和氢氧化钠之间反应生成偏铝酸钠和氢气,根据氢气的体积计算金属铝的质量;
(2)金属铝和氧化铁的混合物反应生成金属铁和氧化铝,根据铝的物质的量计算出氧化铁的质量,然后得出铝和氧化铁的总质量;根据化合价变化判断氧化铝的作用;
(3)氧化铝、铁都能够与盐酸反应,分别写出反应的离子方程式.
解答 解:(1)铝热剂是金属铝和氧化铁的混合物,金属铝可以和氢氧化钠之间反应生成偏铝酸钠和氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知,当生成的氢气(标准状况,下同)体积为6.72L时,生成氢气的物质的量为:$\frac{6.72L}{22.4L/mol}$=0.3mol,则样品中Al的质量为:0.3mol×$\frac{2}{3}$×27g/mol=5.4g,
故答案为:5.4;
(2)铝与氧化铁反应的方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,由于恰好完全反应,其中铝的物质的量是0.3mol×$\frac{2}{3}$=0.2mol,则氧化铁的物质的量为:0.2mol×$\frac{1}{2}$=0.1mol,其质量为:160g/mol×0.1mol=16g;则铝和氧化铁的总质量为:5.4g+16g=21.4g;
该反应中,Al2O3为Al被氧化生成的产物,属于氧化产物,
故答案为:21.4;氧化产物;
(3)氧化铝与盐酸反应生成氯化铝和水,反应的离子方程式为:Al2O3+6H+=2Al3++3H2O,铁与盐酸反应生成氯化亚铁和氢气,反应的离子方程式为:Fe+2H+=Fe2++H2↑、
故答案为:Fe+2H+=Fe2++H2↑、Al2O3+6H+=2Al3++3H2O.
点评 本题考查了混合物反应的计算,题目难度中等,明确铝热反应原理为解答关键,注意熟练掌握物质的量与摩尔质量、气体摩尔体积之间的关系,试题培养了学生的化学计算能力.

| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 2:1 |
| A. | 5.1g | B. | 10.2g | C. | 13.6g | D. | 15.3g |
| A. | 对农作物秸秆进行焚烧还田,以增加土壤肥力 | |
| B. | 推广使用无磷洗衣粉,以减少水体富营养化 | |
| C. | 改进汽车尾气净化技术,减少大气污染物的排放 | |
| D. | 研发可降解高分子材料,减少“白色污染” |
| A. | 沸点:NH3>H2O>H2S | |
| B. | 酸性:H2SO4>HClO4>H3PO3 | |
| C. | 结合质子的能力:CO32->ClO->CH3COO- | |
| D. | 气态氢化物的热稳定性:H2O>HF>NH3 |
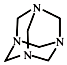
| A. | 化学式为C6H12N4,属于饱和烃 | |
| B. | 不能发生加成反应,一氯取代产物有3种 | |
| C. | 分子中既含极性共价键又含非极性共价键 | |
| D. | 可由甲醛(HCHO)与氨气按物质的量之比3:2完全反应制得 |