题目内容
17.下列图示与对应的叙述相符的是( )
| A. | 图1表示0.1000mol•L-1NaOH溶液滴定20.00ml 0.1000 mol•L-1醋酸溶液得到滴定曲线 | |
| B. | 图2所示在H2S溶液导电性实验中,曲线可确定通入的气体X为Cl2 | |
| C. | 图3在其它条件不变时,2SO2(g)+O2(g)?2SO3(g)转化关系中,纵坐标表示O2的转化率 | |
| D. | 由图4所示曲线可知,酶催化比化学催化的效果好 |
分析 A.醋酸为弱酸,没有滴入氢氧化钠溶液时,0.1000mol/L的醋酸溶液的pH大于1;
B.H2S+Cl2=S↓+2HCl反应弱电解质变化为强电解质,溶液导电能力增大;
C.由图象可知$\frac{n({O}_{2})}{n(S{O}_{2})}$越大,氧气转化率越大,实际应是$\frac{n({O}_{2})}{n(S{O}_{2})}$越大,SO2的转化率越大,氧气转化率越小;
D.催化剂是降低反应的活化能加快反应速率.
解答 解:A.0.1000mol•L-1NaOH溶液滴定20.00mL 0.1000mol•L-1CH3COOH溶液,消氢氧化钠溶液体积为0时,醋酸为弱电解质,醋酸溶液的pH大于1,图象中醋酸的pH=1与实际不符,故A错误;
B.通入的气体X为Cl2反应,H2S+Cl2=S↓+2HCl中物质变化,弱电解质变化为强电解质,溶液导电能力增大,故B错误;
C.由图象可知$\frac{n({O}_{2})}{n(S{O}_{2})}$越大,氧气转化率越大,由反应2SO2(g)+O2(g)?2SO3(g),$\frac{n({O}_{2})}{n(S{O}_{2})}$越大,SO2的转化率越大,氧气转化率越小,图象与实际不相符,故C错误;
D.催化剂是降低活化能加快反应速率,酶催化作用对活化能降低的多,催化效果好,故D正确;
故选D.
点评 本题以图象的形式考查平衡移动、酸性比较、对反应速率的理解等,难度中等,需要学生具有扎实的基础与读图获取信息的能力.

练习册系列答案
相关题目
8.硫元素在周期表中的位置是( )
| A. | 第二周期 VIA族 | B. | 第三周期 VIA族 | C. | 第二周期ⅦA族 | D. | 第三周期 IVA族 |
5.下列有关基本营养物质的说法中,错误的是( )
| A. | 淀粉遇碘化钾溶液变蓝 | |
| B. | 葡萄糖和果糖互为同分异构体 | |
| C. | 利用油脂在碱性条件下水解可制取肥皂 | |
| D. | 用灼烧并闻气味的方法鉴别羊毛织物和棉织物 |
12.A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,而辛是由C元素形成的单质,已知:甲+乙═丁+辛,甲+丙═戊+辛;丁由两种10电子粒子形成,则下列说法正确的是( )
| A. | 元素C形成的单质可以在点燃条件分别与元素A、B、D形成的单质化合,所得化合物均存在共价键 | |
| B. | 元素B、C、D的原子半径由大到小的顺序为:r(D)>r(C)>r(B) | |
| C. | 往1.0 L 0.1 mol•L-1戊溶液中逐滴滴入同浓度的盐酸,立即产生大量气泡 | |
| D. | 1 mol甲与足量的乙完全反应共转移约1.204×l024个电子 |
9.下列离子中,电子数大于质子数,且质子数大于中子数的是( )
| A. | OH- | B. | Mg2+ | C. | OD- | D. | D3O+ |
6.下列反应中,水作还原剂的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | 2F2+2H2O═4HF+O2 | D. | SO2+H2O═H2SO3 |
1.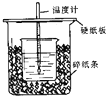 (1)在如图所示的装置中,50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行中和反应,通过测定该反应过程中所放出的热量可计算中和热.回答下列问题:
(1)在如图所示的装置中,50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行中和反应,通过测定该反应过程中所放出的热量可计算中和热.回答下列问题:
①从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所测得的中和热的数值会偏小(填“偏大”“偏小”“无影响”).
(2)某探究实验小组的同学,在进行高锰酸钾酸性溶液与草酸溶液的反应时,发现刚开始的一段时间,反应速率较慢,溶液褪色不明显,但不久后褪色速度明显加快,最后紫红色完全消失.已知草酸与高锰酸钾酸性溶液的反应为:
2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2+8H2O
该小组探究后一阶段褪色速度明显加快的原因:
①设计对比实验:室温下,在三支试管中各加入4mL0.01mol•L-1KMnO4酸性溶液和2mL0.1mol•L-1H2C2O4溶液,再对应加入固体粉末,记录褪色时间.实验数据如下:
设计该实验的目的及实验得出的结论分别是:探究后一阶段褪色速度明显加快的原因;Mn2+作催化剂,加快反应速率;.
②理论分析:依据该反应的原理,推测反应可能是放热反应,温度影响了反应的速率.请你设计一个简单的实验来验证该推测.你的实验操作是:取一支试管,向其中各加入4mL0.01mol•L-1KMnO4酸性溶液和2mL0.1mol•L-1H2C2O4溶液,然后放入冰水混合物中,观察褪色时间.
(3)某研究发现O3氧化海水中的I-是大气中碘的主要来源.通过将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,为测定生成I2的量,用酸式滴定管取20.00mL反应后的溶液与锥形瓶中,用cmol•L-1的Na2S2O3标准液滴定,消耗V mL Na2S2O3溶液.
已知:Ⅰ.H2S2O3是一种弱酸;Ⅱ.2Na2S2O3+I2═Na2S4O6+2NaI
①该滴定实验中除烧杯、锥形瓶、酸式滴定管外,还需要的玻璃仪器是碱式滴定管;
②该滴定实验中可选用淀粉作指示剂(填物质名称);
③实验测得溶液中碘的含量为6.35cVg•L-1(用含c和V的关系式表示).
 (1)在如图所示的装置中,50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行中和反应,通过测定该反应过程中所放出的热量可计算中和热.回答下列问题:
(1)在如图所示的装置中,50mL0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液进行中和反应,通过测定该反应过程中所放出的热量可计算中和热.回答下列问题:①从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所测得的中和热的数值会偏小(填“偏大”“偏小”“无影响”).
(2)某探究实验小组的同学,在进行高锰酸钾酸性溶液与草酸溶液的反应时,发现刚开始的一段时间,反应速率较慢,溶液褪色不明显,但不久后褪色速度明显加快,最后紫红色完全消失.已知草酸与高锰酸钾酸性溶液的反应为:
2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2+8H2O
该小组探究后一阶段褪色速度明显加快的原因:
①设计对比实验:室温下,在三支试管中各加入4mL0.01mol•L-1KMnO4酸性溶液和2mL0.1mol•L-1H2C2O4溶液,再对应加入固体粉末,记录褪色时间.实验数据如下:
| 实验序号 | A | B | C |
| 加入试剂 | KMnO4、H2C2O4 | KMnO4、H2C2O4 1gMnSO4粉末 | KMnO4、H2C2O4 1gNa2SO4粉末 |
| 完全褪色时间/s | 116 | 6 | 117 |
②理论分析:依据该反应的原理,推测反应可能是放热反应,温度影响了反应的速率.请你设计一个简单的实验来验证该推测.你的实验操作是:取一支试管,向其中各加入4mL0.01mol•L-1KMnO4酸性溶液和2mL0.1mol•L-1H2C2O4溶液,然后放入冰水混合物中,观察褪色时间.
(3)某研究发现O3氧化海水中的I-是大气中碘的主要来源.通过将O3通入稀硫酸酸化的NaI溶液中进行模拟研究,为测定生成I2的量,用酸式滴定管取20.00mL反应后的溶液与锥形瓶中,用cmol•L-1的Na2S2O3标准液滴定,消耗V mL Na2S2O3溶液.
已知:Ⅰ.H2S2O3是一种弱酸;Ⅱ.2Na2S2O3+I2═Na2S4O6+2NaI
①该滴定实验中除烧杯、锥形瓶、酸式滴定管外,还需要的玻璃仪器是碱式滴定管;
②该滴定实验中可选用淀粉作指示剂(填物质名称);
③实验测得溶液中碘的含量为6.35cVg•L-1(用含c和V的关系式表示).
