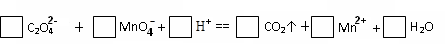��Ŀ����
ȡ10 mL 0.4 mol��L��1 FeCl3��Һ�����ձ��У������м���һ������Fe��Cu������ַ�Ӧ������������һ������ȷ����(����Һ������䣬������ˮ������)
����A���ձ�����Cu��Fe,��Ӧ����Һ��c(Fe2��)��0.6 mol��L��1
����B���ձ�����Fe��Cu,��Ӧ����Һ��c(Fe2��)��0.6 mol��L��1
����C���ձ���Fe��Cu����,��Ӧ����Һ��c(Cl��)��1.2 mol��L��1
����D���ձ���Fe��Cu���У���Ӧ����Һ��c(Fe2��)��0.6 mol��L��1
B
��������

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�����̼ѭ��������������ҵĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2����Ϊ��ѧ���о�����Ҫ���⡣
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ɸ÷�Ӧ�Ļ�ѧ����ʽ��
___ C+ ___ KMnO4+ ____ H2SO4��____CO2��+ ____MnSO4 + ____K2SO4+ ____H2O
��2������ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO(g)��H2O(g) CO2(g)��H2(g)���õ������������ݣ�
CO2(g)��H2(g)���õ������������ݣ�
|
ʵ���� |
�¶ȡ� |
��ʼ��/mol |
ƽ����/mol |
�ﵽƽ������ ʱ��/min |
||
|
CO |
H2O |
H2 |
CO |
|||
|
1 |
650 |
4 |
2 |
1��6 |
2��4 |
6 |
|
2 |
900 |
2 |
1 |
0��4 |
1��6 |
3 |
|
3 |
900 |
a |
b |
c |
d |
t |
��ʵ��2������ƽ�ⳣ��K= ��
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a/b ��ֵ______(�����ֵ��ȡֵ��Χ)��
��ʵ��4����900��ʱ���ڴ������м���CO��H2O��CO2 ��H2��Ϊ1mol�����ʱV�� V�����<�� ����>�� ����=������
��3����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) �� 3O2(g) �� 2CO2(g) �� 4H2O(g) ��H����1275.6 kJ��mol
�� 2CO (g)+ O2(g) �� 2CO2(g) ��H����566.0 kJ��mol
�� H2O(g) �� H2O(l) ��H����44.0 kJ��mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��____________
��4����֪������һ�ֶ�Ԫ���ᣬ�������ƣ�NaHC2O4����Һ�����ԡ������£���10 mL 0.01 mol��L-1 H2C2O4��Һ�еμ�10mL 0.01mol��L-1 NaOH��Һʱ���Ƚ���Һ�и�������Ũ�ȵĴ�С��ϵ ��
��5��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��
CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ1��10-4mo1/L �������ɳ�������CaCl2��Һ����СŨ��Ϊ mo1/L ��
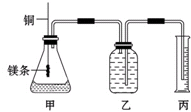 ij�о���ѧϰС��Ϊ֤����ͬ��ͬѹ�£���ͬŨ����ͬ����IJ�ͬǿ�ȵ�һԪ��������þ��Ӧʱ�����������������ͬ����Ӧ���ʲ�ͬ��ͬʱ�ⶨʵ���������µ�����Ħ���������Ƶļ���ʵ��װ����ͼ����ʵ�����Ҫ�����������£�
ij�о���ѧϰС��Ϊ֤����ͬ��ͬѹ�£���ͬŨ����ͬ����IJ�ͬǿ�ȵ�һԪ��������þ��Ӧʱ�����������������ͬ����Ӧ���ʲ�ͬ��ͬʱ�ⶨʵ���������µ�����Ħ���������Ƶļ���ʵ��װ����ͼ����ʵ�����Ҫ�����������£� 4�֣���֪������һ�ֶ�Ԫ���ᣬ�������ƣ�NaHC2O4����Һ�����ԡ�
4�֣���֪������һ�ֶ�Ԫ���ᣬ�������ƣ�NaHC2O4����Һ�����ԡ� L 0.01 mol/L NaHC2O4��Һ�еμ�10mL 0.01 mol/L NaOH��Һʱ���Ƚ���Һ�и�������Ũ�ȵĴ�С��ϵ���ã����ӣ� ��
L 0.01 mol/L NaHC2O4��Һ�еμ�10mL 0.01 mol/L NaOH��Һʱ���Ƚ���Һ�и�������Ũ�ȵĴ�С��ϵ���ã����ӣ� ��