题目内容
【题目】如下图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法正确的是( )

A. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. C(s,石墨)===C(s,金刚石) ΔH=+1.9 kJ·mol-1
【答案】D
【解析】试题分析:从图看出石墨的总能量比金刚石低,石墨的总键能较高,所以1 mol石墨的总键能比1 mol金刚石的总键能大1.9 kJ,A错;石墨和金刚石是不同的物质,石墨和金刚石的转化是化学变化,B错;石墨的总能量较低,物质的总能量越低,物质越稳定,故石墨比金刚石稳定,C错;石墨总能量低,石墨转化为金刚石是吸热反应,D对。

 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案【题目】CoCl2· 6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、 Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2· 6H2O的工艺流程如下:
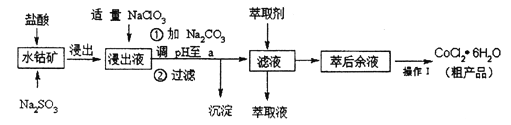
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co (OH) 2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2· 6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中主要发生的离子反应方程式:______________。
(2)若不慎向“浸出液”中加过量NaC1O3时,可能会生成的有害气体是_______(填化学式)。
(3)萃取剂对金属离子的萃取率与pH的关系如图,向“滤液”中加入萃取剂的目的是_______,其使用的最佳pH范围是 ________(选填下列字母)。

A. 2.0~2.5 B. 3.0~3.5 C. 4.0~4.5 D. 5.0~5.5
(4) “操作1”是________。制得的CoCl2· 6H2O需减压烘干的原因是__________。
(5)为测定粗产品中CoCl2· 6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2· 6H2O的质量分数大于100%,其原因可能是___________________。(答一条即可)

