题目内容
10.用Na2SO3溶液吸收硫酸工业尾气中的SO2,Na2SO3+SO2+H2O═2NaHSO3,所得混合液可电解循环再生(A为阳离子交换膜;B为阴离子交换膜).相关物料的传输与转化关系如图.下列说法不正确的是( )
| A. | Pt(Ⅱ)为阳极 | B. | 阳极区酸性增强 | ||
| C. | 图中的n<m | D. | 阴极电极反应式为2H++2e-═H2↑ |
分析 由装置图可知,阳离子向Pt(Ⅰ)电极移动,阴离子向Pt(Ⅱ)移动,且Pt(I)极氢离子转化为氢气,因此Pt(Ⅰ)为阴极,Pt(Ⅱ)为阳极,所以X为直流电源的负极,Y为直流电源的正极,阴极电极反应式为:2H++2e-═H2↑,阳极反应式为:HSO3-+H2O-2e-=SO42-+3H+,SO32-+H2O-2e-=SO42-+2H+,据此分析解答.
解答 解:A.由装置图可知,阳离子向Pt(Ⅰ)电极移动,阴离子向Pt(Ⅱ)移动,且Pt(I)极氢离子转化为氢气,因此Pt(Ⅰ)为阴极,Pt(Ⅱ)为阳极,故A正确;
B.阳极发生氧化反应,阳极反应式为:HSO3-+H2O-2e-=SO42-+3H+,SO32-+H2O-2e-=SO42-+2H+,阳极区酸性增强,故B正确;
C.阳极有硫酸生成,电解质溶液中硫酸浓度增大,故的n>m,故C错误;
D.阳极发生还原反应,氢离子在阴极放电生成氢气,阴极电极反应式为:2H++2e-═H2↑,故D正确,
故选:C.
点评 本题考查电解原理及其应用,关键是根据离子移动与微粒变化判断两极,理解掌握电解工作原理与电极判断方法,较好的考查学生获取信息与知识迁移应用,题目难度不大.

练习册系列答案
相关题目
1.下列离子方程式书写正确的是( )
| A. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,2Fe2++4Br-+3Cl2═2Fe2++2Br2+6Cl- | |
| B. | NaOH溶液与SO2反应,当n(NaOH):n(SO2)=4:3时,4OH-+3SO2═SO32-+2HSO3-+H2O | |
| C. | 酚酞滴入碳酸钠溶液中,溶液变红:CO32-+H2O═HCO3-+OH- | |
| D. | 将铝条投入NaOH溶液中:Al+OH-+H2O═AlO2-+H2↑ |
15.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | pH=1的溶液:Ag+、Al3+、Cl-、SO42- | |
| B. | 能使酚酞试液变红的溶液:Na+、K+、HCO3-、S2- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10-12的溶液:NH4+、Cu2+、NO3-、Cl- | |
| D. | 水电离产生的c(OH-)=10-12 mol•L-1的溶液:K+、Fe2+、SO42-、NO3- |
2.从下列事实所列出的相应结论正确的是( )
| 实 验 事 实 | 结 论 | |
| ① | Cl2的水溶液可以导电 | Cl2是电解质 |
| ② | 将烧红的铁片插入水中生成氢气 | 还原性:Fe>H2 |
| ③ | 向久置空气的漂白粉中加盐酸有CO2气体产生 | 酸性:H2CO3>HClO |
| ④ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色溶液中加入氢氧化钠浓溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定含有NH4+ |
| A. | ③④⑤ | B. | ②③⑤ | C. | ①②③ | D. | 全部 |
19.自然界各种原生铜的硫化物经氧化、淋滤后变成CuSO4溶液,并向深部渗透时,遇到闪锌矿(ZnS)和方铅矿(PbS),便慢慢地转变为铜蓝(CuS),下列有关该过程的解释及说法不合理的是( )
| A. | 原生铜的硫化物具有还原性 | |
| B. | 常温时ZnS、PbS、CuS都难溶于水,CuSO4可溶于水 | |
| C. | 铜蓝的形成过程是:ZnS(S)+Cu2+?CuS(S)+Zn2+ | |
| D. | 硝酸型酸雨不利于铜蓝的形成:CuS+2H+═Cu2++H2S↑ |
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.0 g H218O与D2O的混合物中所含中子数为NA | |
| B. | 常温常压下4.4 g乙醛所含σ键数目为0.7NA | |
| C. | 标准状况下,5.6 L CO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 50 mL 12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
 A是一种重要的化工原料,用来衡量一个国家的石油化工发展水平,相同条件下存在如下转化关系(部分反应物、反应条件和产物已省略),其中E为具有果香气味的物质,F是高聚物.
A是一种重要的化工原料,用来衡量一个国家的石油化工发展水平,相同条件下存在如下转化关系(部分反应物、反应条件和产物已省略),其中E为具有果香气味的物质,F是高聚物.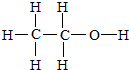 ;写出其官能团的电子式
;写出其官能团的电子式 ,1个该官能团含有9个电子,氢氧根与其组成元素相同,电子式为
,1个该官能团含有9个电子,氢氧根与其组成元素相同,电子式为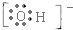 ,含有有10个电子;高聚物F是常用的塑料之一,它的链节可表示为-CH2CH2-.
,含有有10个电子;高聚物F是常用的塑料之一,它的链节可表示为-CH2CH2-.