题目内容
11.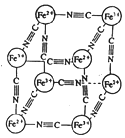 分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )
分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )| A. | 该晶体中含有共价键,是离子晶体 | |
| B. | M 离子位于晶胞面心,呈+2 价 | |
| C. | M 离子位于晶胞体心,呈+1 价,且 M+空缺率为 50%(体心中没有 M+占总体心的百分比) | |
| D. | 晶体的化学式可表示为 MFe2(CN)6,且 M 为+1 价 |
分析 A、该晶体中含有Fe2+、Fe3+、CN-等阴阳离子,CN-中C、N之间为共价键,据此判断晶体类型;
B、根据晶胞结构,利用均摊法确定晶胞中各离子个数,再根据化合价代数各为零可判断;
C、根据晶胞结构,利用均摊法确定晶胞中各离子个数比可判断;
D、根据晶胞结构,利用均摊法确定晶胞中各离子个数,再根据化合价代数各为零可判断.
解答 解:A、该晶体中含有Fe2+、Fe3+、CN-等阴阳离子,所以该晶体为离子晶体,但CN-中C、N之间为共价键,则该晶体中含有共价键,是离子晶体,故A正确;
B、根据晶胞结构可知,晶胞中含有Fe2+的个数为4×$\frac{1}{8}$=$\frac{1}{2}$,Fe3+的个数为4×$\frac{1}{8}$=$\frac{1}{2}$,CN-的个数为12×$\frac{1}{4}$=3,所以Fe2+、Fe3+、CN-的个数比为1:1:6,根据化合价代数和为零可知,M的化合价为+1价,故B错误;
C、根据晶胞结构,由B的计算可知,每个晶胞中含有Fe2+0.5个,Fe3+0.5个,CN-3个,由B可知M的化合价为+1价,根据化合价代数为零,可知每个晶胞平均含有M也是0.5个,而M的离子位于上述立方体的体心上,所以两个晶胞中一个有M+,而另一个必无M+,所以M+空缺率为50%,故C正确;
D、由B的分析可知,晶体的化学式可表示为MFe2(CN)6,且M为+1价,故D正确;
故选B.
点评 本题主要考查均摊法计算化学式、晶体结构的确定等知识点,中等难度,有一定的综合性.

练习册系列答案
相关题目
3. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,再用待测溶液润洗后,注入待测溶液,然后调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③用蒸馏水将锥形瓶洗净后,从碱式滴定管中放入20.00mL待测溶液,滴入甲基橙作指示剂,然后用标准盐酸进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL;
④重复以上过程,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中溶液的颜色从黄色变为橙色时,停止滴定.
(2)图1中,第②步“调节滴定管的尖嘴部分充满溶液”方法正确的是②,如果滴定前有气泡,滴定后气泡消失,由此对测定结果形成的影响是偏高(填“偏高”、“偏低”或“无影响”)
(3)图2中是某次滴定时的滴定管中的液面,其读数为23.60mL.
(4)根据下列数据:
请计算待测烧碱溶液的浓度为0.1200mol/L.
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净,再用待测溶液润洗后,注入待测溶液,然后调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③用蒸馏水将锥形瓶洗净后,从碱式滴定管中放入20.00mL待测溶液,滴入甲基橙作指示剂,然后用标准盐酸进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL;
④重复以上过程,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中溶液的颜色从黄色变为橙色时,停止滴定.
(2)图1中,第②步“调节滴定管的尖嘴部分充满溶液”方法正确的是②,如果滴定前有气泡,滴定后气泡消失,由此对测定结果形成的影响是偏高(填“偏高”、“偏低”或“无影响”)
(3)图2中是某次滴定时的滴定管中的液面,其读数为23.60mL.
(4)根据下列数据:
| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 24.10 |
| 第二次 | 20.00 | 3.00 | 27.10 |
2.下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是( )
| A. | 将少量浓氨水滴入Al2(SO)4溶液 将少量Al2(SO4)3溶液滴入浓氨水 | |
| B. | 将少量SO2通入Ba(OH)2溶液 将过量SO2通入少量Ba(OH)2溶液 | |
| C. | 将0.1molCl2通入含0.2molFeBr2的溶液中 将0.3molCl2通入含0.2molFeBr2溶液 | |
| D. | 将过量BaCl2溶液与少量Na2SO4溶液相混合 将少量Ba(OH)2溶液与过量MgSO4溶液相混合 |
19. 氟的单质及其化合物在工农业生产中应用非常广泛.回答下列问题:
氟的单质及其化合物在工农业生产中应用非常广泛.回答下列问题:
(1)基态氟原子的外围电子排布式为2s22p5,元素周期表中氟元素所在的区为p.
(2)电解NaHF2(氟化氢钠)可制氟气.NaHF2中所含作用力的类型有离子键、共价键、氢键,与HF2-互为等电子体的分子是CO2(或Na2O)(任写一种).
(3)OF2是一种氧化性极强的气体,其中氧原子的杂化轨道类型是sp3.
(4)部分氟化物的熔点和莫氏硬度的数据如表:
①NaF的熔点高于SiF4的原因是NaF为离子晶体,SiF4为分子晶体,由于离子键比分子间作用力强得多,故NaF的熔点高于SiF4
②MgF2的莫氏硬度大于NaF的原因是MgF2和NaF都是离子晶体,它们的阴离子都是F-,而Mg2+的半径比Na+小,Mg2+所带电荷数比Na+多,则MgF2晶格能大于NaF,故MgF2的莫氏硬度大于NaF
(5)氟化钙的晶胞结构如图所示,晶胞参数a=0.555nm.
①Ca2+、F-的配位数分别为8、4.
②列式计算氟化钙晶体的密度:ρ=$\frac{4×78}{{N}_{A}•(5.55×1{0}^{-6})^{3}}$(不必计算出结果,用NA表示阿伏加德罗常数的数值)g•cm-3.
 氟的单质及其化合物在工农业生产中应用非常广泛.回答下列问题:
氟的单质及其化合物在工农业生产中应用非常广泛.回答下列问题:(1)基态氟原子的外围电子排布式为2s22p5,元素周期表中氟元素所在的区为p.
(2)电解NaHF2(氟化氢钠)可制氟气.NaHF2中所含作用力的类型有离子键、共价键、氢键,与HF2-互为等电子体的分子是CO2(或Na2O)(任写一种).
(3)OF2是一种氧化性极强的气体,其中氧原子的杂化轨道类型是sp3.
(4)部分氟化物的熔点和莫氏硬度的数据如表:
| 化合物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
| 莫氏硬度 | 3.2 | 6.0 | 无 |
②MgF2的莫氏硬度大于NaF的原因是MgF2和NaF都是离子晶体,它们的阴离子都是F-,而Mg2+的半径比Na+小,Mg2+所带电荷数比Na+多,则MgF2晶格能大于NaF,故MgF2的莫氏硬度大于NaF
(5)氟化钙的晶胞结构如图所示,晶胞参数a=0.555nm.
①Ca2+、F-的配位数分别为8、4.
②列式计算氟化钙晶体的密度:ρ=$\frac{4×78}{{N}_{A}•(5.55×1{0}^{-6})^{3}}$(不必计算出结果,用NA表示阿伏加德罗常数的数值)g•cm-3.
6.甲、乙两种非金属,能说明甲比乙的非金属性强的是( )
①甲比乙的单质容易与H2化合 ②甲单质能与乙的简单阴离子发生置换反应 ③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强 ④与某金属反应时,甲原子得电子数目比乙的多 ⑤甲的单质熔、沸点比乙的低.
①甲比乙的单质容易与H2化合 ②甲单质能与乙的简单阴离子发生置换反应 ③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强 ④与某金属反应时,甲原子得电子数目比乙的多 ⑤甲的单质熔、沸点比乙的低.
| A. | 全部 | B. | 只有⑤ | C. | ①②③ | D. | ①②③④ |
16.建筑用红砖中含有Fe2O3,若要检验红砖中+3价铁元素的存在,应该选用的试剂及其顺序为( )
(供选择的试剂:①KSCN溶液②H2O2溶液③盐酸④酸性KMnO4溶液)
(供选择的试剂:①KSCN溶液②H2O2溶液③盐酸④酸性KMnO4溶液)
| A. | ①④ | B. | ③① | C. | ③②① | D. | ③①④ |
3.下列解释事实的离子方程式不正确的是( )
| A. | Na放入水中,产生气体:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | FeCl3溶液滴在淀粉碘化钾试纸上,试纸变蓝:2Fe3++2I-═2Fe2++I2 | |
| C. | 铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O | |
| D. | 氯气溶于水:Cl2+H2O?H++Cl-+HClO |
20.下列物质转化在给定条件下能实现的是( )
| A. | FeS2$\stackrel{煅烧}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | NaCl(aq)$\stackrel{电解}{→}$Na$\stackrel{点燃}{→}$Na2O2 | |
| C. | Fe$\stackrel{稀H_{2}SO_{4}}{→}$FeSO4(aq)$\stackrel{NaOH}{→}$Fe(OH)2$\stackrel{空气中的灼烧}{→}$Fe2O3 | |
| D. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(aq)$\stackrel{Cu}{→}$Fe |
1.如图所示装置,有关说法错误的是( )
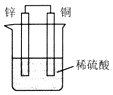

| A. | 锌是负极,其质量逐渐减少 | |
| B. | 电子由铜片经导线流向锌片 | |
| C. | H+在铜片表面被还原,产生气泡 | |
| D. | 锌片上发生氧化还原,铜片上发生还原反应 |