题目内容
4.硅是无机非金属材料的主角之一.下列关于硅及其化合物性质的说法,不正确的是( )| A. | 硅的非金属性比硫弱 | B. | 硅酸钠可溶于水 | ||
| C. | SiO2与氢氟酸能反应 | D. | 硅原子易失去或得到电子 |
分析 A、同周期从左到右非金属性逐渐增强;
B、钠盐都溶于水;
C、二氧化硅与氢氟酸反应生成四氟化硅和水;
D、硅原子最外层4个电子.
解答 解:A、同周期从左到右非金属性逐渐增强,所以硅的非金属性比硫弱,故A正确;
B、钠盐都溶于水,则硅酸钠可溶于水,故B正确;
C、二氧化硅与氢氟酸反应生成四氟化硅和水,所以SiO2与氢氟酸能反应,故C正确;
D、硅原子最外层4个电子,既难失电子又难得电子,故D错误;
故选D.
点评 本题考查了硅及其化合物的性质,难度不大,明确硅的原子结构是解答选项D的关键.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
14.下列物质既能发生消去反应又能被氧化成醛的是( )
| A. | (CH3)3CCH2OH | B. | 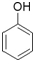 | C. | 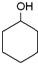 | D. | (CH3)2CBrCH2OH |
15.硫酸亚铁是重要的亚铁盐,广泛用于医药、化工和防腐等领域.
(1)硫酸亚铁溶液呈酸性,其原因是Fe2++2H2O?Fe(OH)2+2H+(用离子方程式表示).
(2)硫酸亚铁在高温下会发生分解.某化学学习小组为探究硫酸亚铁在不同温度下的分解产物,进行了如下探究.请你完成下列问题:
【提出猜想】
①硫酸亚铁在不同温度下分解得到产物,可能是FeO和SO3(沸点44.8℃);也可能是Fe2O3、SO3和SO2.
【实验探究】
小组的同学根据猜想,设计了实验装置,并选择了可能用到的试剂如下:
A.品红溶液、B.KSCN溶液、C.BaCl2溶液 D.Ba(NO3)2溶液.
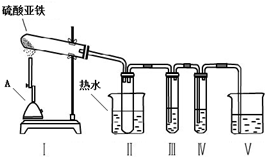
②为了得到较高温度,加热用的仪器A名称是酒精喷灯.
③为了检验气体产物中含有SO3,在装置Ⅲ应装的试剂是C(选填试剂序号),装置Ⅱ中装热水的作用是避免SO3冷却成液体.
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
⑤若生成的固体产物为Fe2O3和FeO,且其物质的量相等.则反应的化学方程式为3FeSO4 $\frac{\underline{\;高温\;}}{\;}$FeO+Fe2O3+SO2↑+2SO3↑.
(1)硫酸亚铁溶液呈酸性,其原因是Fe2++2H2O?Fe(OH)2+2H+(用离子方程式表示).
(2)硫酸亚铁在高温下会发生分解.某化学学习小组为探究硫酸亚铁在不同温度下的分解产物,进行了如下探究.请你完成下列问题:
【提出猜想】
①硫酸亚铁在不同温度下分解得到产物,可能是FeO和SO3(沸点44.8℃);也可能是Fe2O3、SO3和SO2.
【实验探究】
小组的同学根据猜想,设计了实验装置,并选择了可能用到的试剂如下:
A.品红溶液、B.KSCN溶液、C.BaCl2溶液 D.Ba(NO3)2溶液.

②为了得到较高温度,加热用的仪器A名称是酒精喷灯.
③为了检验气体产物中含有SO3,在装置Ⅲ应装的试剂是C(选填试剂序号),装置Ⅱ中装热水的作用是避免SO3冷却成液体.
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
| 操作步骤 | 预期实验现象 | 预期实验结论 |
| 向其中一份溶液中加入 KSCN溶液(或B). | 溶液变成血红色 | 固体中含有Fe2O3 |
| 向另一份溶液中滴加 2滴黄色K3[Fe(CN)6]溶液. | 产生蓝色沉淀 | 固体中含有FeO |
12.牛肉和菠菜等食物中含有丰富的铁,这里的“铁”应理解为( )
| A. | 单质 | B. | 分子 | C. | 原子 | D. | 元素 |
19.组成为C6H4S4的物质有吸收微波的功能,可在军事上用做隐形飞机的涂层.下列关于C6H4S4的说法不正确的是( )
| A. | 该物质为有机物 | B. | 该物质为无机物 | ||
| C. | 该物质由三种元素组成 | D. | 该物质燃烧产物可能含CO2 |
9.出土的铜器文物表面有一层绿色的铜锈,铜锈的主要成分是( )
| A. | 碱式碳酸铜 | B. | 碳酸铜 | C. | 氢氧化铜 | D. | 氧化铜 |
16.下列物质中,不能与稀盐酸反应的有( )
| A. | Cu | B. | CaCO3 | C. | Zn | D. | AgNO3 |
13.氨气与氧气在有催化剂的条件下进行反应,不会发生的现象是( )
| A. | 产生的气体溶于水中,能使酚酞变红 | |
| B. | 催化剂保持红热 | |
| C. | 可能生成红棕色的气体 | |
| D. | 可能产生白烟 |
7.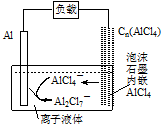 最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )
最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )
 最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )
最近中美研究人员发明了一种可快速充放电的铝离子电池,该电池电解质为离子液体{AlCl3/[EMIM]Cl},放电时有关离子转化如图所示.下列说法正确的是( )| A. | 充电时,阴极发生:4Al2Cl7-+3e-═Al+7AlCl4- | |
| B. | 充电时,泡沫石墨极与外电源的负极相连 | |
| C. | 放电时,负极发生:2AlCl4--e-═Al2Cl7-+Cl- | |
| D. | 放电时,电路中每流过3mol电子,正极减少27g |