题目内容
海水资源丰富,海水中主要含有Na+、K+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子.合理利用海水资源和保护环境是我国可持续发展的重要保证.
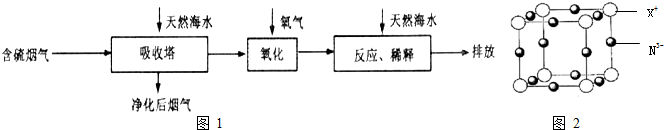
Ⅰ.火力发电燃煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如图1所示:
(1)天然海水显碱性的原因是(用离子方程式表示): .
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是 ;氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是 .
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.0,ρ≈1g?mL-1)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(3)你认为往废水中投入 (填字母序号),沉淀效果最好.
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)= .
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×l0-8mol?L-1,问该工厂处理后的废水中c(Ag+)= ,是否符合排放标准 (填“是”或“否”).已知Ksp(AgCl)=1.8×l0-10.
Ⅰ.火力发电燃煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如图1所示:

(1)天然海水显碱性的原因是(用离子方程式表示):
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,其反应的化学方程式是
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.0,ρ≈1g?mL-1)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol?L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| KSP | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
(5)如果用食盐处理其只含Ag+的废水,测得处理后的废水中NaCl的质量分数为0.117%.若环境要求排放标准为c(Ag+)低于1.0×l0-8mol?L-1,问该工厂处理后的废水中c(Ag+)=
考点:盐类水解的应用,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:I(1)海水中的弱酸根离子水解显碱性;
(2)H2SO3或HSO3-中的S显+4价,均可被O2氧化生成H++SO42-,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+);
II(3)溶度积越小越易转化为沉淀,根据表格中的数据进行判断最近试剂;
(4)先计算出溶液中氢氧根离子的物质的量浓度,然后根据Pb(OH)2的溶度积及c(Pb2+)=
进行计算;
(5)根据氯化银的溶度积进行解答,并与排放标准对比来说明是否符合排放标准.
(2)H2SO3或HSO3-中的S显+4价,均可被O2氧化生成H++SO42-,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+);
II(3)溶度积越小越易转化为沉淀,根据表格中的数据进行判断最近试剂;
(4)先计算出溶液中氢氧根离子的物质的量浓度,然后根据Pb(OH)2的溶度积及c(Pb2+)=
| Ksp |
| c2(OH-) |
(5)根据氯化银的溶度积进行解答,并与排放标准对比来说明是否符合排放标准.
解答:
解:I(1)天然海水的pH≈8,是因为海水中有CO32-或HCO3-+它们水解使海水呈弱碱性,其离子方程式为CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-,故答案为:CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-;
(2)H2SO3中的S显+4价,均可被O2氧化生成H2SO4,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+),
故答案为:2H2SO3+O2=2H2SO4;中和、稀释经氧气氧化后海水中生成的酸(H+);
II(3)溶度积越小的越易转化为沉淀,由表格中的数据可知,硫化物的溶度积小,则应选择硫化钠,
故答案为:B;
(4)由Pb(OH)2的溶度积为1.2×10-15,pH=8.0,c(OH-)=10-6mol?L-1,则c(Pb2+)=
=
=1.2×10-3mol?L-1,
故答案为:1.2×10-3mol?L-1;
(5)废水中NaCl的质量分数为0.117%(ρ≈1g?mL-1),c(Cl-)=c(NaCl)=
=0.02mol/L,
Ksp(AgCl)=c(Ag+)?c(Cl-)=1.8×10-10mol2?L-2,则c(Ag+)=
=9×10-9mol?L-1,环境要求排放标准为c(Ag+)低于1.0×10-8mol?L-1,显然9×10-9mol?L-1<1.0×l0-8mol?L-1,则符合排放标准,
故答案为:9×10-9mol?L-1;是.
(2)H2SO3中的S显+4价,均可被O2氧化生成H2SO4,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+),
故答案为:2H2SO3+O2=2H2SO4;中和、稀释经氧气氧化后海水中生成的酸(H+);
II(3)溶度积越小的越易转化为沉淀,由表格中的数据可知,硫化物的溶度积小,则应选择硫化钠,
故答案为:B;
(4)由Pb(OH)2的溶度积为1.2×10-15,pH=8.0,c(OH-)=10-6mol?L-1,则c(Pb2+)=
| Ksp |
| c2(OH-) |
| 1.2×10-15 |
| (10-6)2 |
故答案为:1.2×10-3mol?L-1;
(5)废水中NaCl的质量分数为0.117%(ρ≈1g?mL-1),c(Cl-)=c(NaCl)=
| 1000×1g/mL×0.117% |
| 58.5g/mol |
Ksp(AgCl)=c(Ag+)?c(Cl-)=1.8×10-10mol2?L-2,则c(Ag+)=
| 1.8×10-10 |
| 0.02 |
故答案为:9×10-9mol?L-1;是.
点评:本题考查了含硫烟气的处理及难溶物的沉淀转化,利用所学知识结合框图信息是解答本题的关键,难度中等,注意把握Ksp的有关计算的方法.

练习册系列答案
相关题目
工业合成SO3的反应为2SO2(g)+O2(g)?2SO3(g)△H<0,下列能使平衡向正反应方向移动的是( )
| A、加入催化剂 |
| B、升温 |
| C、充入一定量的O2 |
| D、减小压强 |
下列离子方程式中,正确的是( )
| A、铁与盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
| B、氯气与氯化亚铁溶液反应:2FeCl2+Cl2═2FeCl3 |
| C、氯化铁溶液与铁反应:Fe3++Fe═2Fe2+ |
| D、氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-═Fe(OH)3↓ |
