题目内容
15.标准状况下,8.0g O2的体积为( )| A. | 22.4 L | B. | 11.2 L | C. | 8.0 L | D. | 5.6 L |
分析 根据n=$\frac{m}{M}$计算氧气物质的量,根据V=nVm计算混合气体标准状况下体积.
解答 解:8g O2的物质的量为n=$\frac{m}{M}$=$\frac{8g}{32g/mol}$=0.25mol,则O2在标准状况下氧气的体积为V=nVm=0.25mol×22.4L/mol=5.6L,
故选D.
点评 本题考查物质的量计算,比较基础,难度不大,注意掌握以物质的量为中心计算.

练习册系列答案
相关题目
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 7.8g苯中含有C-C单键数目为0.3NA | |
| B. | 标准状况下,2.24L的CHCl3中含有的C-H键数为0.1NA | |
| C. | 1.4g C2H4和C3H8的混合物中含碳原子数为0.1 NA | |
| D. | 13克溶有乙炔的苯乙烯,其所含的电子数目为7 NA |
6.下列物质的电子式正确的是( )
| A. | 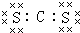 | B. | 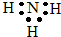 | C. | 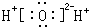 | D. | 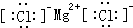 |
3.下列实验现象,是由于发生加成反应而引起的是( )
| A. | 乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 苯与溴水混合,反复振荡后溴水层颜色变浅 | |
| C. | 油脂使溴的四氯化碳溶液褪色 | |
| D. | 甲烷与氯气混合,光照一段时间后黄绿色消失 |
10.通常把拆开1mol某化学键所吸收的能量看成该化学键的键能.已知部分化学键的键能如下:
(1)发射神舟飞船的长征火箭用了肼(N2H4,气态)为燃料,若它在氧气(气态)中燃烧,生成N2(气态)和H2O(液态).1mol肼完全燃烧时放出的热量为577kJ.
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH 溶液.肼-空气燃料电池放电时,正极的电极反应式是O2+2H2O+4e-=4OH-.
(3)已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有90个N-N键.
| 化学键 | N-H | N-N | O═O | N≡N | O-H |
| 键能 (kJ•mol-1) | 386 | 167 | 498 | 946 | 460 |
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH 溶液.肼-空气燃料电池放电时,正极的电极反应式是O2+2H2O+4e-=4OH-.
(3)已知N60分子中每个N原子均以氮氮键结合三个氮原子,且N60分子结构中每个氮原子均形成8个电子的稳定结构.试推测1个N60的结构含有90个N-N键.
20.下列化合物中含有2个手性碳原子的是( )
| A. | 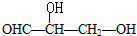 | B. | 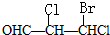 | ||
| C. | CH3CH2COOH | D. | 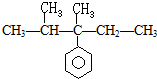 |
4.下列物质属于电解质的是( )
| A. | Cl2 | B. | NH3 | C. | FeSO4 | D. | 蔗糖 |
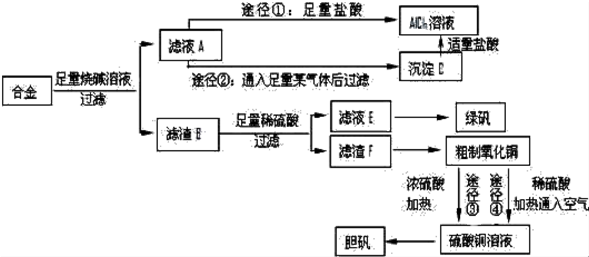
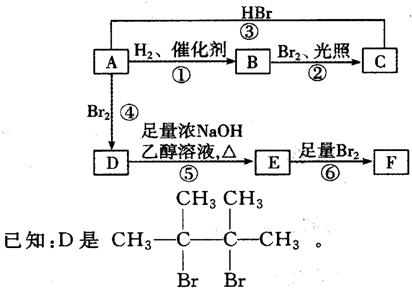
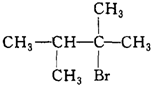 .
. ;;写出由E-F的化学方程式
;;写出由E-F的化学方程式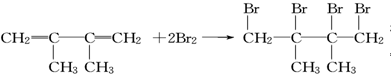 .
.