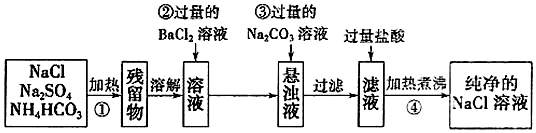
题目内容
15.常温下,取铝土矿(含有Al2O3、FeO、Fe2O3、SiO2等物质)用硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中能大量共存的一组离子正确的是( )| A. | 加入过量NaOH溶液:Na+、AlO2-、OH-、SO42- | |
| B. | 加入过量氨水:NH4+、Al3+、OH-、SO42- | |
| C. | 通入过量Cl2:Fe2+、Na+、Cl-、SO42- | |
| D. | 通入过量SO2:Fe2+、H+、SO32-、SO42- |
分析 取铝土矿(含有Al2O3、FeO、Fe2O3、SiO2等物质)用硫酸浸出后的溶液,含Al3+、Fe2+、Fe3+,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:A.硫酸浸出后的溶液,含Al3+、Fe2+、Fe3+,加入过量NaOH,Fe2+、Fe3+转化为沉淀,溶液中含Na+、AlO2-、OH-、SO42-,故A正确;
B.加入过量氨水不能大量存在Al3+,故B错误;
C.通入过量Cl2与Fe2+发生氧化还原反应,不能共存,故C错误;
D.通入过量SO2与SO32-反应,不能大量存在SO32-,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
5.如表是元素周期表的一部分,表中所列的字母分别代表某一化学元素
(1)表中所列元素中属于主族元素的有a、b、c、d、f、g、h、i、j、k、l;属于金属元素的有b、c、d、e、f、h;e在元素周期表中的位置是第四周期 VIII族.
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
| a | ||||||||||||||||||
| g | j | |||||||||||||||||
| b | c | f | i | l | m | |||||||||||||
| e | h | k | ||||||||||||||||
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
6.下列反应的离子方程式书写正确的是( )
| A. | 铁粉与稀H2SO4反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Na2CO3溶液与足量盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | Cu(OH)2固体与稀硫酸反应:OH-+H+═H2O | |
| D. | 铝片与NaOH溶液反应:Al+OH-+H2O═AlO2-+H2↑ |
3. X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
 X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )| A. | Z与M的最高价氧化物对应水化物均为强酸 | |
| B. | X、Y、Z三种元素组成的化合物可能是酸、碱或盐 | |
| C. | 简单离子半径:M>Y>Q | |
| D. | 电解RM2水溶液可得到R单质 |
20..某校化学兴趣小组探究SO2的一些性质.
[探究一]:SO2能否被BaCl2溶液吸收.
甲.乙两同学分别设计如图装置甲和装置乙进行探究
甲、乙两同学实验时观察到各仪器中的现象如下:
回答下列问题:
(1)甲同学经过后续实验确证了B中白色沉淀是BaSO4.甲同学的后续实验操作是打开B试管的胶塞,向其中滴加稀盐酸,若白色沉淀不消失,证明白色沉淀是BaSO4

(2)乙同学分析装置甲中产生BaSO4的可能原因有:
①A中产生的白雾是硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀.
②2SO2+O2+2H2O+2Ba2+=2BaSO4+4H+(用离子方程式表示).
(3)装置乙中B中所盛试剂是饱和NaHSO3溶液;乙同学在滴加浓硫酸之前的操作是打开弹簧夹向A中通往一段时间的N2,然后关闭弹簧夹
(4)通过上述实验,得出的结论是SO2不能被BaCl2溶液吸收
[探究二]:SO2与FeCl3溶液的反应
查阅资料:①Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+;②生成Fe(HSO3)2+离子的反应为可逆反应.实验步骤为:
回答下列问题:
(5)当SO2通入到FeCl3(未用盐酸酸化)溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象.将混合液放置12小时,溶液才变成浅绿色.
则溶液由棕黄色变成红棕色的原因是二氧化硫溶于水SO2+H2O?HSO3-+H+,Fe3++HSO3-?Fe(HSO3)2+;写出溶液由红棕色变为浅绿色时发生反应的离子方程式Fe3++Fe(HSO3)2++H2O=2Fe2++SO42-+3H+
(6)通过实验可知加热和增加FeCl3溶液的酸度可缩短浅绿色出现的时间.
[探究一]:SO2能否被BaCl2溶液吸收.
甲.乙两同学分别设计如图装置甲和装置乙进行探究
甲、乙两同学实验时观察到各仪器中的现象如下:
| A | B | C | D | |
| 装置甲中的现象 | Na2SO3固体表面有气泡.瓶中白雾 | 白色沉淀 | ----- | ------ |
| 装置乙中的现象 | Na2SO3固体表面有气泡.瓶中白雾 | 有气泡 | 有气泡 | 品红褪色 |
(1)甲同学经过后续实验确证了B中白色沉淀是BaSO4.甲同学的后续实验操作是打开B试管的胶塞,向其中滴加稀盐酸,若白色沉淀不消失,证明白色沉淀是BaSO4

(2)乙同学分析装置甲中产生BaSO4的可能原因有:
①A中产生的白雾是硫酸的酸雾,进入B中与BaCl2溶液反应生成BaSO4沉淀.
②2SO2+O2+2H2O+2Ba2+=2BaSO4+4H+(用离子方程式表示).
(3)装置乙中B中所盛试剂是饱和NaHSO3溶液;乙同学在滴加浓硫酸之前的操作是打开弹簧夹向A中通往一段时间的N2,然后关闭弹簧夹
(4)通过上述实验,得出的结论是SO2不能被BaCl2溶液吸收
[探究二]:SO2与FeCl3溶液的反应
查阅资料:①Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+;②生成Fe(HSO3)2+离子的反应为可逆反应.实验步骤为:
| 步骤I | 往5mL1mol•L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色.微热3min,溶液颜色变为浅绿色. |
| 步骤II | 往5mL重新配制的1mol•L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色.几分钟后,发现溶液颜色变成浅绿色. |
(5)当SO2通入到FeCl3(未用盐酸酸化)溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象.将混合液放置12小时,溶液才变成浅绿色.
则溶液由棕黄色变成红棕色的原因是二氧化硫溶于水SO2+H2O?HSO3-+H+,Fe3++HSO3-?Fe(HSO3)2+;写出溶液由红棕色变为浅绿色时发生反应的离子方程式Fe3++Fe(HSO3)2++H2O=2Fe2++SO42-+3H+
(6)通过实验可知加热和增加FeCl3溶液的酸度可缩短浅绿色出现的时间.
7.下列化学实验事实及其结论都正确的是( )
| 选项 | 实验事实 | 结论 |
| A | 二氧化硅可以和NaOH溶液及HF溶液反应 | 二氧化硅属于两性氧化物 |
| B | SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑ | 酸性:H2SiO3>H2CO3 |
| C | 向氯化铝溶液中滴加氢氧化钠溶液,观察到先产生白色沉淀后沉淀溶解 | 氢氧化铝可溶于强碱 |
| D | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝的熔点髙 |
| A. | A | B. | B | C. | C | D. | D |
4.下列装置不能达到除杂目的(括号内为杂质)的是( )
| A. |  乙烷(乙烯) | B. |  苯(甲苯) | C. | 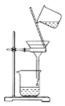 溴苯(CaO) | D. | 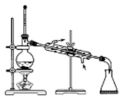 I2(CCl4) |
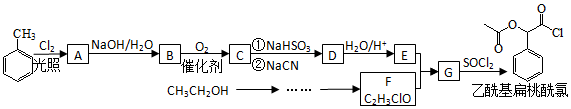
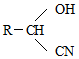 ;RCN$\stackrel{H_{2}O/H+}{→}$RCOOH;RCOOH$\stackrel{SOCl}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′
;RCN$\stackrel{H_{2}O/H+}{→}$RCOOH;RCOOH$\stackrel{SOCl}{→}$RCOCl$\stackrel{R′OH}{→}$RCOOR′