题目内容
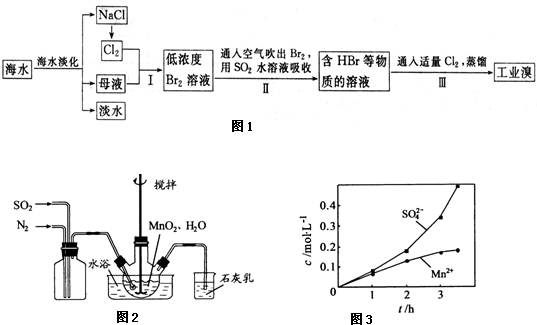
Ⅰ.海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列.从海水中提取食盐和溴的过程如图1:
(1)请列举海水淡化的两种方法: 、 .
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 .
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为: ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 .
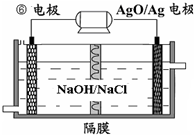
Ⅱ.高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如图2:
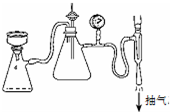
(1)制备MnSO4溶液:在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3═MnSO4+H2O)
①反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有 、 .
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t的浓度变化如图3.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是 .
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7,请补充由(1)时制得的MnSO4制备高纯MnCO3的操作步骤.①边搅拌边加入 ,并控制溶液pH ;② ;③检验SO42-是否被洗涤除去;④用少量 洗涤;⑤低于100℃干燥.

(1)请列举海水淡化的两种方法:
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为:
Ⅱ.高纯MnCO3是制备高性能磁性材料的主要原料.实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如图2:
(1)制备MnSO4溶液:在烧瓶中(装置见右图)加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h.停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3═MnSO4+H2O)
①反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t的浓度变化如图3.导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7,请补充由(1)时制得的MnSO4制备高纯MnCO3的操作步骤.①边搅拌边加入
考点:海水资源及其综合利用,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:Ⅰ、(1)海水淡化的方法有:蒸馏、渗析等方法;
(2)海水淡化得到的母液和电解氯化钠溶液生成的氯气反应,得到的溴单质浓度低,溴单质在水中有一定的溶解性且和水反应,提取时消耗过的能源和原料,降低了经济效益;
(3)溴和二氧化硫发生氧化还原反应生成氢溴酸和硫酸;
Ⅱ、(1)①根据实验的操作原则,为了让气体尽可能转化,要根据反应所需的条件和用量严格操作;
②考虑氮气的化学性质稳定,空气中氧气的活泼性等因素的影响;
(2)根据题干中所给的试剂结合MnCO3的性质来选择合适的制取方案.
(2)海水淡化得到的母液和电解氯化钠溶液生成的氯气反应,得到的溴单质浓度低,溴单质在水中有一定的溶解性且和水反应,提取时消耗过的能源和原料,降低了经济效益;
(3)溴和二氧化硫发生氧化还原反应生成氢溴酸和硫酸;
Ⅱ、(1)①根据实验的操作原则,为了让气体尽可能转化,要根据反应所需的条件和用量严格操作;
②考虑氮气的化学性质稳定,空气中氧气的活泼性等因素的影响;
(2)根据题干中所给的试剂结合MnCO3的性质来选择合适的制取方案.
解答:
解:Ⅰ.(1)目前淡化海水的方法有多种,如:蒸留法、电渗析法、离子交换法、溶剂萃取法和冰冻法等,
故答案为:蒸馏法;电渗析法、离子交换法(任意两种);
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,目的是低浓度的Br2溶液在提取时消耗过多的原料和能源,转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素;故答案为:富集溴元素;
(3)步骤II为二氧化硫和溴的氧化还原反应,反应的离子方程式为Br2+SO2+2H2O=4H++SO42-+2Br-,由此反应可知,生成物为强酸,所以除环境保护外,在工业生产中应解决的主要问题是强酸对设备的严重腐蚀;
故答案为:Br2+SO2+2H2O=4H++SO42-+2Br-;强酸对设备的严重腐蚀;
Ⅱ.(1)①为使SO2尽可能转化完全,应定要保证控制反应的温度,在通入SO2和N2比例一定、不改变固液投料的条件下,要求所通气体一定要慢,故答案为:控制适当的温度;缓慢通入混合气体;
②氮气的化学性质稳定,空气中氧气性质活泼,在Mn2+催化作用下,易把亚硫酸氧化成硫酸,而使硫酸根浓度增大,故答案为:Mn2+催化氧气与亚硫酸反应生成硫酸;
(2)制取的原理是碳酸根和锰离子之间反应生成碳酸锰的过程,但要考虑MnCO3难溶于水、乙醇并在潮湿时易被空气氧化,100℃开始分解以及Mn(OH)2开始沉淀时pH=7.7等因素,过程中控制溶液的PH值以及洗涤沉淀所选的溶剂要小心,边搅拌边加入碳酸钠或碳酸氢钠,并控制溶液的PH<7.7、过滤,用水洗涤2-3次、检验SO42-是否被除去、用少量的乙醇洗涤;
故答案为:NaHCO3(Na2CO3);<7.7;过滤,用少量水洗涤2~3次;C2H5OH.
故答案为:蒸馏法;电渗析法、离子交换法(任意两种);
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,目的是低浓度的Br2溶液在提取时消耗过多的原料和能源,转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素;故答案为:富集溴元素;
(3)步骤II为二氧化硫和溴的氧化还原反应,反应的离子方程式为Br2+SO2+2H2O=4H++SO42-+2Br-,由此反应可知,生成物为强酸,所以除环境保护外,在工业生产中应解决的主要问题是强酸对设备的严重腐蚀;
故答案为:Br2+SO2+2H2O=4H++SO42-+2Br-;强酸对设备的严重腐蚀;
Ⅱ.(1)①为使SO2尽可能转化完全,应定要保证控制反应的温度,在通入SO2和N2比例一定、不改变固液投料的条件下,要求所通气体一定要慢,故答案为:控制适当的温度;缓慢通入混合气体;
②氮气的化学性质稳定,空气中氧气性质活泼,在Mn2+催化作用下,易把亚硫酸氧化成硫酸,而使硫酸根浓度增大,故答案为:Mn2+催化氧气与亚硫酸反应生成硫酸;
(2)制取的原理是碳酸根和锰离子之间反应生成碳酸锰的过程,但要考虑MnCO3难溶于水、乙醇并在潮湿时易被空气氧化,100℃开始分解以及Mn(OH)2开始沉淀时pH=7.7等因素,过程中控制溶液的PH值以及洗涤沉淀所选的溶剂要小心,边搅拌边加入碳酸钠或碳酸氢钠,并控制溶液的PH<7.7、过滤,用水洗涤2-3次、检验SO42-是否被除去、用少量的乙醇洗涤;
故答案为:NaHCO3(Na2CO3);<7.7;过滤,用少量水洗涤2~3次;C2H5OH.
点评:本题以海水资源综合利用为载体考查了氧化还原反应、物质的分离和提纯、工艺流程等知识点,学生分析和解决问题的能力,能从整体上把握工艺流程,知道物质间的反应、每一步的目的,题目难度中等.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
化学式为C4H8的链状烃有(考虑顺反异构体)( )
| A、3种 | B、4种 | C、5种 | D、6种 |
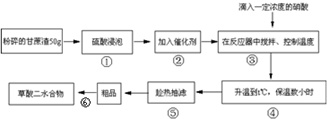
 步骤⑥采用的操作方法是:
步骤⑥采用的操作方法是: