题目内容
由M层有2个电子的元素X与L层有5个电子的元素Y形成的化合物的化学式为( )
| A、XY |
| B、X2Y3 |
| C、X3Y2 |
| D、X2Y5 |
考点:原子核外电子排布,根据化合价正确书写化学式(分子式)
专题:
分析:M层有2个电子的元素X,即易失去这2个电子显+2价,L层有5个电子的元素Y,易得到3个电子显-3价,据此分析.
解答:
解:M层有2个电子的元素X,即易失去这2个电子显+2价,L层有5个电子的元素Y,易得到3个电子显-3价,所以形成的化合物的化学式为X3Y2;
故选:C.
故选:C.
点评:本题难度不大,考查了利用化合价确定化学式的方法,注意根据最外层电子数确定化合价即可解题;

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用水稀释0.1mol?L-1氨水时,溶液中随加入水的体积增加而减小的是( )
| A、c(H+) |
| B、c(NH3?H2O) |
| C、c(H+)和c(OH-)的乘积 |
| D、OH-的物质的量 |
500K时,有CO催化剂加氢反应:CO(g)+3H2(g)?CH4(g)+H2O(g)△H<0,下列有关说法正确的是( )
| A、温度升高时,该反应的平衡常数K增大 |
| B、缩小容器体积,平衡体系中各物质的浓度均增大 |
| C、温度越低,越有有利于CO催化氢 |
| D、从平衡体系中分离出H2O(g)能加快正反应速率 |
实验表明,在一定条件下,乙烯和水反应可表示为:C2H4(g)+H2O(g)═C2H5OH(g)△H=-45.8kJ/mol
则下列说法中正确的是( )
则下列说法中正确的是( )
| A、实验中,乙烯的用量不会影响该反应的反应焓变△H |
| B、0.5molH2O(l)完全反应放出的热量为22.9kJ |
| C、1molC2H5OH(g)具有的能量大于1molC2H4(g)和1molH2O(g)所具有的能量和 |
| D、1molC2H4(g)和1molH2O (g)中化学键的总键能大于1molC2H5OH(g)中化学键的总键能 |
已知298K时,2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q1;向另一体积相同的密闭容器中通入1molSO2和0.5molO2,达到平衡时放出热量Q2.则下列关系式正确的是( )
| A、2Q2=Q1 | ||
| B、2Q2<Q1 | ||
| C、Q2<Q1=197kJ | ||
D、Q2=
|
下列离子方程式正确的是( )
A、用惰性电极电解饱和氯化钠溶液:2Cl-+2H+
| ||||
B、氯气通入浓氢氧化钠溶液中加热:3Cl2+6OH-
| ||||
| C、用稀硝酸溶解FeS固体:FeS+2H+═Fe2++H2S↑ | ||||
| D、硫酸氢钠溶液与足量氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
在一条件下,可逆反应2A(气)+B(气)?n(C)(固)+D(气)
达到平衡.若维持温度不变,增大强压,测得混合气体的平均相对分子质量不发生改变,则下列判断正确的是( )
达到平衡.若维持温度不变,增大强压,测得混合气体的平均相对分子质量不发生改变,则下列判断正确的是( )
| A、其它条件不变,增大压强,平衡不发生移动 | ||||
| B、其它条件不变,增大压强,混合气体的总质量不变 | ||||
C、反应可以从正反应开始,也可以从逆反应开始,但必须满足下列条件:其中x、y、z分别表示第一次达到平衡时,A、B、D的物质的量(mol),(其中M表示物质的摩尔质量,下同)
| ||||
D、反应只能从正反应开始,且原混合气中A与B的物质的量之比为2:1,并有
|
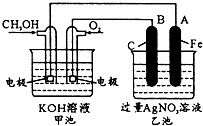 如图是一个化学过程的示意图.已知甲池的总反应式为:
如图是一个化学过程的示意图.已知甲池的总反应式为: