题目内容
10.葡萄可用于酿酒.(1)检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2,加热,其现象是产生砖红色沉淀.
(2)有机物E由碳、氢、氧三种元素组成,可由葡萄糖发酵得到,也可从酸牛奶中提取,纯净的E为无色粘稠液体,易溶于水.为研究E的组成与结构,通过实验得到如下信息:
①有机物E的相对分子量为90.9.0g E完全燃烧时,生成CO2 0.3mol,H2O5.4g.则有机物E的分子式为C3H6O3.
②实验证实其中含有羟基,羧基,甲基,则E的结构简式为CH3CH(OH)COOH.
③写出E与足量Na的化学方程式CH3CH(OH)COOH+2Na→CH3CH(ONa)COONa+H2↑.
分析 (1)葡萄糖中含有醛基,能被新制的氢氧化铜悬浊液氧化,所以实验现象是产生砖红色沉淀;
(2)该有机物相对分子质量为90,该有机物完全燃烧生成二氧化碳与水,生成CO2 0.3mol,H2O5.4g,根据原子守恒确定分子中C、H原子数目,依据相对分子质量结合质量守恒计算分子中氧原子数目,进而确定分子式;结合分子式确定其结构简式,E含有羟基、羧基两官能团都能与钠反应生成氢气.
解答 解:(1)葡萄糖中含有醛基,能被新制的氢氧化铜悬浊液氧化,所以实验现象是产生砖红色沉淀氧化亚铜,
故答案为:产生砖红色沉淀;
(2)①该有机物的相对分子质量为90,生成的二氧化碳的物质的量为0.3mol,生成的水的质量为5.4g,水的物质的量为$\frac{5.4g}{18g/mol}$=0.3mol;有机物E的物质的量为 n=$\frac{m}{M}$=$\frac{9g}{90g/mol}$=0.1mol,故分子中N(C)=$\frac{0.3mol}{0.1mol}$=3、N(H)=$\frac{0.3mol×2}{0.1mol}$=6,则分子中N(O)=$\frac{90-12×3-6}{16}$=3,故有机物E的分子式为C3H6O3,
故答案为:C3H6O3;
②经红外光谱测定,证实其中含有羟基(-OH),羧基(-COOH),甲基(-CH3),则E的结构简式为:CH3CH(OH)COOH,
故答案为:CH3CH(OH)COOH;
③E与足量Na,羟基、羧基两官能团都能与钠反应,化学方程式为:CH3CH(OH)COOH+2Na→CH3CH(ONa)COONa+H2↑,
故答案为:CH3CH(OH)COOH+2Na→CH3CH(ONa)COONa+H2↑.
点评 本题考查有机物分子式与结构简式确定、官能团的检验等,注意掌握燃烧法利用原子守恒确定有机物分子式,题目难度中等.

| A. | 溶液的体积:10V甲≤V乙 | |
| B. | 水电离出的OH-浓度:10c(OH-)甲=c(OH-)乙 | |
| C. | 若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙 | |
| D. | 若分别与5mLpH=11的NaOH溶液反应,所得溶液的pH:甲≤乙 |
| A. | CH≡CH和CH2═CH-CH═CH2 | B. | CH3-CH═CH2和CH3-CH2-CH═CH2 | ||
| C. | CH3-CH3和CH3-CH═CH2 | D. | 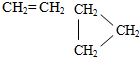 |

| A. | 该有机物属于饱和链烃 | |
| B. | 该有机物可由两种单炔烃分别与氢气加成得到 | |
| C. | 该烃与2,3-二甲基丁烷互为同系物 | |
| D. | 该烃的一氯取代产物共有5种 |
| A. | 单位时间生成n mol A2同时生成n mol AB | |
| B. | 容器内总压不随时间变化 | |
| C. | 单位时间生成2n mol AB同时生成n mol B2 | |
| D. | 混合气体的平均相对分子质量不随时间变化 |
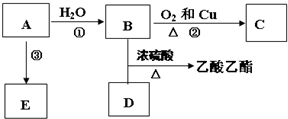
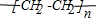 ,E不能(填“能”或“不能”)使酸性KMnO4溶液褪色.
,E不能(填“能”或“不能”)使酸性KMnO4溶液褪色.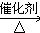 2CH3CHO+2H2O,反应类型氧化反应;B+DCH3COOH+C2H5OH
2CH3CHO+2H2O,反应类型氧化反应;B+DCH3COOH+C2H5OH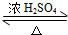 CH3COOC2H5+H2O,反应类型酯化(或取代)反应.
CH3COOC2H5+H2O,反应类型酯化(或取代)反应.
