题目内容
用NA表示阿伏伽德罗常数的数值,下列叙述正确的是( )
| A、常温下,1mol丙烯中含碳原子数为3NA |
| B、常温下,pH=13的NaOH溶液中含OH-数为NA |
| C、标准状况下,22.4LCHCl3中含C-H键数为NA |
| D、23gNa与足量氧气反应时转移的电子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、一个丙烯分子含有3个碳原子;
B、溶液体积不知不能计算微粒数;
C、标准状况下,22.4LCHCl3不是气体;
D、23gNa的物质的量为1mol,完全反应失去电子数为NA.
B、溶液体积不知不能计算微粒数;
C、标准状况下,22.4LCHCl3不是气体;
D、23gNa的物质的量为1mol,完全反应失去电子数为NA.
解答:
解:A、一个丙烯分子含有3个碳原子,1mol丙烯中含碳原子3mol,碳原子数为3NA,故A正确;
B、常温下,pH=13的氢氧化钠溶液中,溶液体积不知不能计算含OH-数目,故B错误;
C、标准状况下,22.4LCHCl3不是气体,物质的量不是1mol,含C-H键数目不为NA,故C错误;
D、23gNa的物质的量为1mol,完全反应失去电子数为NA,即转移电子数为NA,故D错误;
故选A.
B、常温下,pH=13的氢氧化钠溶液中,溶液体积不知不能计算含OH-数目,故B错误;
C、标准状况下,22.4LCHCl3不是气体,物质的量不是1mol,含C-H键数目不为NA,故C错误;
D、23gNa的物质的量为1mol,完全反应失去电子数为NA,即转移电子数为NA,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积的条件应用,微粒数目的计算方法,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
下列物质中所含原子数相同的是( )
| A、7g N2和标准状况下5.6L CO2 |
| B、标准状况下1mol CO2和22.4L水 |
| C、1mol SO2和 22.4LH2 |
| D、m g O2和m g O3 |
 某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中0点代表氢元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的蜗牛形状,图中每个点代表-种元素,其中0点代表氢元素.下列说法中正确的是( )| A、虚线相连的元素处于同一族 |
| B、离0点越远的元素原子半径越大 |
| C、.B、C最高价氧化物的水化物可相互反应 |
| D、A、B组成的化合物中不可能含有共价键 |
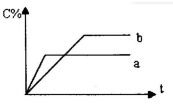 如图表示可逆反应A(g)+B(g)?nC(g)△H<0,在不同条件下反应混合物中C的质量分数C%和反应过程所需时间的关系曲线,有关叙述一定正确的是( )
如图表示可逆反应A(g)+B(g)?nC(g)△H<0,在不同条件下反应混合物中C的质量分数C%和反应过程所需时间的关系曲线,有关叙述一定正确的是( )| A、a表示有催化剂,而b无催化剂 |
| B、若其他条件相同,a比b的温度高 |
| C、若其他条件相同,a比b的压强大,n=l |
| D、反应由逆反应方向开始 |
下列反应中生成物总能量高于反应物总能量的是( )
| A、炭和水蒸气反应 |
| B、乙醇燃烧 |
| C、铝粉与氧化铁粉末反应 |
| D、氧化钙溶于水 |
设计如图所示的装置研究电化学原理,下列叙述错误的是( )
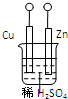

| A、a、b不连接时,只锌片上有气泡逸出,锌片逐渐溶解 |
| B、a和b用导线连接时,H+从铜片上获得锌失去的电子 |
| C、a和b是否用导线连接,装置中所涉及的化学反应都相同 |
| D、a和b是否用导线连接,装置中都是化学能转变为电能过程 |
要使含有Ag+、Cu2+、Mg2+、Ba2+等离子的溶液中的离子逐一形成沉淀析出,下列所选择试剂及加入试剂的顺序正确的是( )
| A、H2SO4→HCl→K2S→NaOH→CO2 |
| B、Na2SO4→NaCl→Na2S→NH3?H2O |
| C、NaCl→Na2SO4→H2S→NaOH |
| D、Na2S→Na2SO4→NaCl→NaOH |
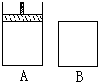 有两只密闭容器A和B,A能保持恒压,B能保持恒容.起始时向容积相等的A、B中分别通入体积比为2:1的等量的SO2和O2,使之发生反应:2SO2+O2?2SO3,并达到平衡.则(填>、=、<;左、右;增大、减小、不变).
有两只密闭容器A和B,A能保持恒压,B能保持恒容.起始时向容积相等的A、B中分别通入体积比为2:1的等量的SO2和O2,使之发生反应:2SO2+O2?2SO3,并达到平衡.则(填>、=、<;左、右;增大、减小、不变).