题目内容
已知下列热化学方程式
2H2(g)+O2(g)=2H2O(1) △H= -571.6KJ/mol
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) △H = -890.3 kJ/mol
1 g 氢气和1 g 甲烷分别燃烧后,放出的热量之比最接近
A.1 : 3.4 B.1 : 1.7 C.2.3 : 1 D.4.6 : 1
C
【解析】
试题分析:1 g 氢气燃烧放出的热量是571.6KJ/4=142.9kJ,1 g 甲烷燃烧放出的热量是890.3 kJ/16=55.6kJ,两者之比为2.6:1最接近2.3:1,答案选C。
考点:燃烧热的计算

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
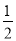 O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1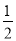 O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1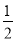 O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1 O2(g)
O2(g) 2H2O(l)+CO(g) ΔH1
2H2O(l)+CO(g) ΔH1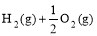 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·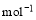
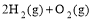 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ·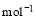
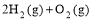 =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·