题目内容
12.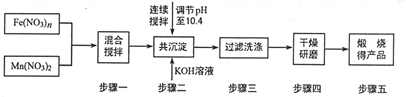 随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:(提示:锰元素在本题所有过程中价态均不变).
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:(提示:锰元素在本题所有过程中价态均不变).(1)推断原料Fe(NO3)n中n=3.
(2)步骤二中“连续搅拌”的目的是充分反应或沉淀完全;写出本步骤涉及所有反应的离子方程式:Fe3++3OH-=2Fe(OH)3↓;Mn2++2OH-=Mn(OH)2↓.
(3)说明步骤三中洗涤干净的标准:取最后一次洗涤液少许,测洗下来的溶液呈中性.
(4)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4$\stackrel{>1000K}{→}$MnFe2O4-x+$\frac{x}{2}$O2↑;MnFe2O4-x+xH2O→MnFe2O4+xH2↑.
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中x=0.6,计算MnFe2O4-x中Fe3+占全部铁元素的百分率=40%.
②该热化学循环制氢法的优点(答两点即可):具有过程简单节约能源无污染物料廉价、可循环使用及氧气和氢气在不同步骤生成,因此不存在高温气体分离等优点.
③该热化学循环法制氢尚有不足之处,指出需要进一步改进的研究方向:寻找合适催化剂使MnFe2O4的分解温度降低或找到分解温度更低的氧化物(答一点即可).
分析 (1)根据MnFe2O4的制备流程,可知Mn、Fe的化合价未变,Mn(NO3)2中Mn的化合价为+2,则MnFe2O4中Fe的化合价为+3,从而求出Fe(NO3)n中的n;
(2)根据搅拌的通常目的和判断沉淀是否洗涤干净的方法来解答,Fe3+和Mn2+在碱性条件下生成沉淀;
(3)原先溶液呈碱性;
(4)①根据铁的总价态不变,用方程组来解决;
②③由流程可看出其优点,改进方法可从流程简洁方面考虑.
解答 解:(1)Mn为+2价,则MnFe2O4中Fe的化合价为+3价,则Fe(NO3)n中n=3,且Fe(NO3)n与Mn(NO3)2 二者之比 2:1,故答案为:3;
(2)连续搅拌是为了让二者充分反应,Fe3+和Mn2+在碱性条件下生成沉淀,离子方程式:Fe3++3OH-=2Fe(OH)3↓;Mn2++2OH-=Mn(OH)2↓,故答案为:充分反应或沉淀完全;Fe3++3OH-=2Fe(OH)3↓;Mn2++2OH-=Mn(OH)2↓;
(3)原先溶液呈碱性,取最后一次洗涤液少许,测洗下来的溶液呈中性,故答案为:取最后一次洗涤液少许,测洗下来的溶液呈中性;
(4)①x=0.6时,铁的总价态为(4-0.6)×2-2=4.8,设1mol MnFe2O4-0.8中含Fe2+、Fe3+物质的量分别为xmol、ymol,则有
x+y=2
2x+3y=4.8
解得:x=1.2,y=0.8,
则1 mol MnFe2O4-0.8中含Fe2+的物质的量为1.2 mol,则Fe2+占的百分率为$\frac{1.2}{2}$×100%=60%,Fe3+占全部铁元素的百分率为40%,故答案为:40%;
②由流程图可以看出过程简单、节约能量、无污染、物料廉价并可循环使用及氧气和氢气在不同步骤生成,不存在高温气体分离的问题等,
故答案为:过程简单、节约能量、无污染、物料廉价并可循环使用及氧气和氢气在不同步骤生成,不存在高温气体分离的问题等(答两点即可);
③因高温消耗较多的能源,则寻找合适的催化剂,使MnFe2O4分解温度降低或分解温度更低的氧化物,故答案为:寻找合适的催化剂,使MnFe2O4分解温度降低或分解温度更低的氧化物.
点评 本题以MnFe2O4的制备为载体,考查学生对工艺流程的理解、对实验操作的理解、化学式有关计算等,难度中等,综合性较强,涉及的知识点多,需要学生具备阅读分析能力和灵活运用知识的解决问题能力.

 名校课堂系列答案
名校课堂系列答案| A. | SO2+H2O═H2SO3 | B. | SO2+2NaOH═Na2SO3+H2O | ||
| C. | 2SO2+O2$\frac{\underline{\;V_{2}O_{5}\;}}{△}$2SO3 | D. | SO2+2H2S═3S↓+2H2O |
| A. | Be、N、F | B. | Mg、Si、C | C. | Na、Mg、Ca | D. | Cl、S、P |
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
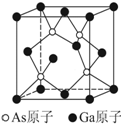 氮族元素和硼族元素在生产生活中有很重要的地位.
氮族元素和硼族元素在生产生活中有很重要的地位.