题目内容
若硬水中钙、镁离子以碳酸氢钙、碳酸氢镁的形式存在,可以通过煮沸使钙、镁离子转化为沉淀.写出这一过程的化学方程式: .
考点:盐类水解的应用,难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:碳酸氢盐可以受热分解为碳酸盐、水以及二氧化碳,碳酸镁的溶解度大于氢氧化镁的溶解度,沉淀向着更难溶的方向转化,据此回答.
解答:
解:碳酸盐热可分解生成碳酸盐、水和二氧化碳,反应的化学方程式为Ca(HCO3)2
CaCO3↓+H2O+CO2↑,Mg(HCO3)2
MgCO3↓+H2O+CO2↑,碳酸镁的溶解度大于氢氧化镁的溶解度,沉淀向着更难溶的方向转化,MgCO3+H2O
Mg(OH)2+CO2↑,故答案为:Ca(HCO3)2
CaCO3↓+H2O+CO2↑,Mg(HCO3)2
MgCO3↓+H2O+CO2↑,MgCO3+H2O
Mg(OH)2+CO2↑.
| ||
| ||
| ||
| ||
| ||
| ||
点评:本题考查学生碳酸氢盐和碳酸盐之间的转化知识,注意知识的归纳和梳理是解题关键,难度中等.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
有关纯碱和小苏打的叙述正确的是( )
| A、向NaHCO3溶液中滴入Ba(OH)2溶液无沉淀,而向Na2CO3溶液中加入Ba(OH)2溶液出现白色沉淀 |
| B、等质量的Na2CO3、NaHCO3分别与足量的同浓度盐酸反应,NaHCO3消耗盐酸体积多 |
| C、等质量的Na2CO3、NaHCO3分别与足量稀H2SO4反应,NaHCO3产生的CO2多 |
| D、Na2CO3和NaHCO3都既能与酸反应,又能与氢氧化钠反应 |
I2(g)+H2(g)?2HI(g)△H<0,在其他条件不变的情况下正确说法是( )
| A、加入催化剂,改变了反应的途径,反应的△H也随之改变 |
| B、改变压强,平衡不发生移动,反应放出的热量不变 |
| C、升高温度,反应速率加快,反应放出的热量变多 |
| D、若在原电池中进行,反应放出的热量不变 |
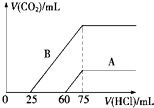 取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题: