题目内容
16.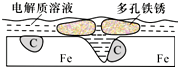 炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑.腐蚀原理如右图所示,下列说法正确的是( )
炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈斑.腐蚀原理如右图所示,下列说法正确的是( )| A. | 腐蚀过程中,负极是C | |
| B. | Fe失去电子经电解质溶液转移给C | |
| C. | 正极的电极反应式为4OH--4e-═2H2O+O2↑ | |
| D. | 每生成1 mol铁锈(Fe2O3•xH2O)理论上消耗标准状况下的O233.6 L |
分析 铁锅中含有Fe、C,Fe、C和电解质溶液构成原电池,中性条件下,钢铁发生吸氧腐蚀,该原电池中,Fe易失电子作负极、C作正极,负极上铁失电子生成亚铁离子,正极上氧气得电子发生还原反应,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,被氧气氧化生成氢氧化铁,分解生成氧化铁结晶水合物生锈,据此分析解答
解答 解:该原电池中,Fe易失电子作负极、C作正极,负极上铁失电子生成亚铁离子,正极上氧气得电子发生还原反应,负极反应式为Fe-2e-=Fe2+、正极反应式为O2+2H2O+4e-=4OH-,
A.分析可知原电池反应,铁做负极被腐蚀,碳做正极,故A错误;
B.原电池中电子沿外导线从负极流向正极,不能通过电解质溶液,电解质溶液中是离子的定向移动形成闭合回路,故B错误;
C.正极电极反应是溶液中氧气得到电子发生还原反应,电极反应O2+2H2O+4e-=4OH-,故C错误;
D.负极反应式为Fe-2e-=Fe2+、正极反应式为O2+2H2O+4e-=4OH-,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,被氧气氧化生成氢氧化铁,离子反应方程式为Fe2++2OH-=Fe(OH)2、化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,每生成1 mol铁锈(Fe2O3•xH2O),铁元素为2mol,依据铁元素守恒计算,
2Fe~O2~2Fe(OH)2~4e-,
2mol 1 mol 2mol
4Fe(OH)2~O2
4 1
2 mol 0.5mol
理论上消耗标准状况下的O2体积=1.5mol×22.4L/mol=33.6 L,故D正确;
故选D.
点评 本题考查了金属的电化腐蚀,电极名称、电极反应、电子流向等原电池的基础知识,主要是氧化还原反应电子守恒的计算,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 伴随有能量变化的物质变化都是化学变化 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 已知相同条件下2SO2(g)+O2(g)?2SO3(g)△H1,反应2SO2(s)+O2(g)?2SO3(g)△H2,则△H1>△H2 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓H2SO4与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
| A. | 15种 | B. | 12种 | C. | 10种 | D. | 9种 |
| A. | 丙酸的结构简式:CH3CH2COOH | B. | 甲烷的结构式:CH4 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 乙醇的结构式: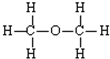 |
| A. | MnO2是还原剂 | B. | MnCl2是氧化产物 | C. | Cl2是氧化产物 | D. | H2O是还原产物 |
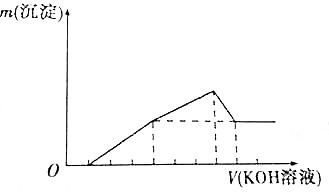 把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )
把镁铝合金用稀H2SO4溶解,加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量之比为( )| A. | 1:1 | B. | 8:9 | C. | 2:3 | D. | 4:3 |
| A. | 制备Al(OH)3悬浊液:向1mol•L-1AlCl3溶液中加过量的6mol•L-1NaOH溶液 | |
| B. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O=[Al(OH)4]-+4NH${\;}_{4}^{+}$ | |
| C. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔纸在酒精灯上加热,溶化后的液态铝滴落下来,金属铝的熔点较低 | |
| D. | 将AlCl3加入Ba(HCO3)2溶液中同时有气体和沉淀产生 |
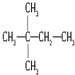 (3)
(3)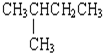 (4)CH3(CH2)3CH3
(4)CH3(CH2)3CH3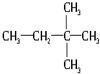 (9)
(9)