题目内容
常温下,一定浓度的某溶液由水电离出的c(OH-)=10-4 mol/L,则该溶液的溶质可能是( )
| A、AlCl3 |
| B、NaOH |
| C、Na2CO3 |
| D、NaHSO4 |
考点:盐类水解的原理,水的电离
专题:
分析:常温下,一定浓度的某溶液由水电离出的c(OH-)=10-4 mol/L>10-7mol/L,说明该物质促进水电离,则为含有弱离子的盐,据此分析解答.
解答:
解:酸或碱抑制水电离,含有弱离子的盐促进水电离,常温下,一定浓度的某溶液由水电离出的c(OH-)=10-4 mol/L>10-7mol/L,说明该物质促进水电离,则为含有弱离子的盐,
A.氯化铝属于强酸弱碱盐,能水解而促进水电离,故A正确;
B.NaOH是碱,抑制水电离,故B错误;
C.碳酸钠是强碱弱酸盐,促进水电离,故C正确;
D.硫酸氢钠是强酸强碱酸式盐,溶液呈强酸性,抑制水电离,故D错误;
故选AC.
A.氯化铝属于强酸弱碱盐,能水解而促进水电离,故A正确;
B.NaOH是碱,抑制水电离,故B错误;
C.碳酸钠是强碱弱酸盐,促进水电离,故C正确;
D.硫酸氢钠是强酸强碱酸式盐,溶液呈强酸性,抑制水电离,故D错误;
故选AC.
点评:本题以盐类水解为载体考查水的电离,明确哪些物质抑制水电离、哪些物质促进水电离即可解答,易错选项是D,注意硫酸氢钠抑制水电离,但弱酸酸式盐能促进水电离,题目难度不大.

练习册系列答案
相关题目
下列粒子的VSEPR模型为四面体,但空间立体构型为V形的是( )
| A、OF2 |
| B、CO2 |
| C、SO2 |
| D、NH4+ |
下列各组离子中,能在溶液中大量共存的是( )
| A、K+ H+ Cl- SO42- |
| B、Ca2+ NO3- HCO3- OH- |
| C、Na+ H+ NO3- Fe2+ |
| D、Fe3+ Cl- H+ CO32- |
某反应:A?B+C 在低温下不能自发进行,在高温下能自发进行,对该反应过程△H、△S的判断正确的是( )
| A、△H<0、△S<0 |
| B、△H>0、△S<0 |
| C、△H<0、△S>0 |
| D、△H>0、△S>0 |
已知2H2(g)+O2(g)=2H2O(g)△H=-484kJ/mol.且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则氢气中1mol H-H键断裂时吸收热量为( )
| A、920 kJ |
| B、557 kJ |
| C、436 kJ |
| D、188 kJ |
室温时,M(OH)2(s)?M2+(aq)+2OH-(aq).Ksp[M(OH)2]=a,c(M2+)=bmol?L-1时,溶液的pH等于( )
A、
| ||||
B、
| ||||
C、14+
| ||||
D、14+
|
对于下列反应类型的判断,不正确的是( )
| A、2FeCl2+Cl2═2FeCl3(化合反应) | ||||
B、3CO+Fe2O3
| ||||
C、2KClO3
| ||||
D、H2CO3
|
下列说法中错误的是( )
| A、根据对角线规则,铍和铝的性质具有相似性 |
| B、[Cu(H2O)4]2+中Cu提供空轨道,H2O中O提供孤对电子形成配位键 |
| C、元素电负性越大的原子,吸引电子的能力越强 |
| D、手性分子互为镜像,它们的性质没有区别 |
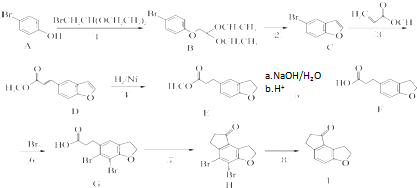
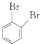 为原料制备
为原料制备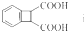 的合成路线流程图(无机试剂任选).(合成路线常用的表示方法为:A
的合成路线流程图(无机试剂任选).(合成路线常用的表示方法为:A