题目内容
3.“分子机器设计和合成”有着巨大的研究潜力.人类步入分子器件时代后,使得光控、温控和电控分子的能力更强,下图是蒽醌套索醚电控开关.下列说法错误的是( )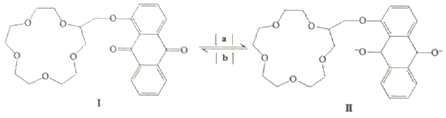
| A. | 物质Ⅰ的分子式是C25H28O8 | B. | 反应是氧化反应 | ||
| C. | 1molⅠ可与8molH2发生加成反应 | D. | 物质Ⅰ的所有原子不可能共平面 |
分析 物质Ⅰ含有C=O、苯环,与氢气发生加成反应生成C-O,为还原反应,含有饱和碳原子,具有甲烷的结构特点,以此解答该题.
解答 解:A.由结构简式可知物质Ⅰ的分子式是C25H28O8,故A正确;
B.物质Ⅰ含有C=O,与氢气发生加成反应生成C-O,为还原反应,故B错误;
C.1molⅠ含有2molC=O键,2mol苯环,则可与8molH2发生加成反应,故C正确;
D.物质Ⅰ含有饱和碳原子,具有甲烷的结构特点,所有原子不可能共平面,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的结构和官能团的性质,难度不大.

练习册系列答案
相关题目
14.本届奥运会上多名运动员因兴奋剂检测呈阳性而使比赛成绩取消,如图是其中检测出的两种兴奋剂的结构:
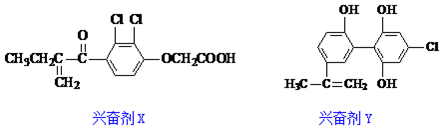
关于它们的说法中正确的是( )
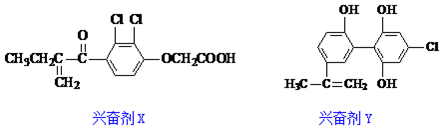
关于它们的说法中正确的是( )
| A. | Y遇到氯化铁溶液时显紫色,但不能使溴的四氯化碳溶液褪色 | |
| B. | X既可以发生氧化反应,又可以发生还原反应 | |
| C. | 1molX与足量氢气反应,最多可消耗6molH2 | |
| D. | 1molY分子中最多有8个碳原子共面 |
18.对某一可逆反应:A+B?2C达到化学平衡,下列说法正确的是( )
| A. | 增加A的量,化学平衡向右移动 | |
| B. | 温度升高,化学平衡一定会发生移动 | |
| C. | 增大压强,缩小容器体积,化学平衡不移动 | |
| D. | 添加MnO2,化学反应速率加快 |
5.未来新能源的特点是资源丰富,在使用过程中对环境无污染或污染很小,且可以再生.下列属于未来新能源开发方向的是 ( )
①天然气 ②煤 ③燃料电池 ④太阳能 ⑤生物质能 ⑥风能 ⑦氢能.
①天然气 ②煤 ③燃料电池 ④太阳能 ⑤生物质能 ⑥风能 ⑦氢能.
| A. | ①②③④ | B. | ③④⑤⑥⑦ | C. | ②③⑤⑥⑦ | D. | ①④⑤⑥⑦ |
12.下列仪器名称为“分液漏斗”的是( )
| A. |  | B. |  | C. |  | D. |  |
9.硼元素的平均相对原子质量为10.8,则硼在自然界中的两种同位素${\;}_{\;}^{10}$B和B${\;}_{\;}^{11}$的原子个数比为( )
| A. | 1:4 | B. | 10:11 | C. | 4:1 | D. | 5:22 |
10.相同条件下,下列气体密度最大的是( )
| A. | 氯气 | B. | 二氧化硫 | C. | 氮气 | D. | 氢气 |