题目内容
CaCO3广泛存在于自然界,是一种重要的![]() 化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。
化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。

完成下列填空:
(1)用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol·L-1),需要的玻璃仪器有 ▲
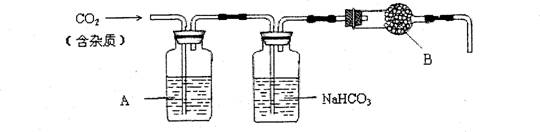
(2)上述装置中,A是 ▲ 溶液,其作用是 ▲ 。
(3)上述装置中,B物质是 ▲ 。
(4)一次性饭盒中石蜡和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重
①从物质分类的角度分析,石蜡属于有机物中的 ▲ 类,为了将石蜡从饭盒中溶出,应选用下列试剂中的 ▲ 。
a.氯化钠溶液 b.稀醋酸 c.稀硫酸 d 正已烷
②饭盒中的碳酸钙常用稀醋酸将其溶出,试写出其反应的离子方程式
▲ 。
(1)烧杯、玻璃棒、量筒;
(2)饱和NaHCO3;吸收HCl气体或吸收酸性气体;
(3)无水CaCl2 或硅胶或P2O5固体;
(4)①烃 , d
② CaCO3+2CH3COOH=2CH3COO-+Ca2++H2O+CO2↑

练习册系列答案
相关题目