题目内容
如图所示,A~J分别表示中学化学中常见的一种物质,其中A为难熔的金属氧化物,可用作耐火材料.B为黑色晶体.它们之间的相互关系如下:
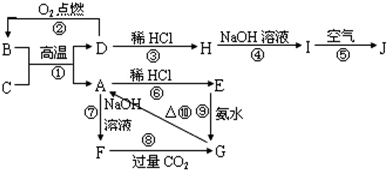
(1)请写出下列物质的化学式:B 、F ;
(2)请写出反应①、⑤的化学方程式:① 、⑤ ;
(3)写出反应⑨的离子方程式 ;
(4)反应⑧除生成G外,还生成的另一溶质是 (填化学式),写出该溶质的一种用途 .

(1)请写出下列物质的化学式:B
(2)请写出反应①、⑤的化学方程式:①
(3)写出反应⑨的离子方程式
(4)反应⑧除生成G外,还生成的另一溶质是
考点:无机物的推断
专题:推断题
分析:A为难熔的金属氧化物,能与NaOH、稀HCl反应,为两性氧化物,则A为Al2O3,由转化关系可知,E为AlCl3,G为Al(OH)3,F为NaAlO2.B为黑色晶体,反应①应为铝热反应,可推知D为Fe、B为Fe3O4,C为Al.Fe与盐酸反应生成H为FeCl2,FeCl2与NaOH溶液反应生成I为Fe(OH)2,在空气中氧化生成J为Fe(OH)3,以此解答该题.
解答:
解:A为难熔的金属氧化物,能与NaOH、稀HCl反应,为两性氧化物,则A为Al2O3,由转化关系可知,E为AlCl3,G为Al(OH)3,F为NaAlO2.B为黑色晶体,反应①应为铝热反应,可推知D为Fe、B为Fe3O4,C为Al.Fe与盐酸反应生成H为FeCl2,FeCl2与NaOH溶液反应生成I为Fe(OH)2,在空气中氧化生成J为Fe(OH)3,
(1)由上述分析可知,B为Fe3O4、F为NaAlO2,
故答案为:Fe3O4;NaAlO2;
(2)反应式①是Al与Fe3O4反应生成Fe与氧化铝,反应方程式为:3Fe3O4+8Al
4Al2O3+9Fe;
反应⑤是Fe(OH)2在空气中氧化生成J为Fe(OH)3,反应方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:3Fe3O4+8Al
4Al2O3+9Fe;4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)反应⑨是氯化铝与氨水反应生成氢氧化铝与氯化铵,反应离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;
(4)反应⑧除生成Al(OH)3外,还生成的另一溶质是碳酸氢钠,可用于制备纯碱或做发酵粉等,故答案为:NaHCO3;制备纯碱或做发酵粉.
(1)由上述分析可知,B为Fe3O4、F为NaAlO2,
故答案为:Fe3O4;NaAlO2;
(2)反应式①是Al与Fe3O4反应生成Fe与氧化铝,反应方程式为:3Fe3O4+8Al
| ||
反应⑤是Fe(OH)2在空气中氧化生成J为Fe(OH)3,反应方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:3Fe3O4+8Al
| ||
(3)反应⑨是氯化铝与氨水反应生成氢氧化铝与氯化铵,反应离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+;
(4)反应⑧除生成Al(OH)3外,还生成的另一溶质是碳酸氢钠,可用于制备纯碱或做发酵粉等,故答案为:NaHCO3;制备纯碱或做发酵粉.
点评:本题考查无机物的推断,为高频考点,“A为主族元素的固态氧化物,能与NaOH、稀HCl反应”是推断的突破口,注意掌握铝热反应,在推断中经常涉及,题目难度中等.

练习册系列答案
相关题目
在11.8g铁铜混合物中加入足量的硝酸,得到硝酸唯一的还原产物NO的物质的量为0.2mol,充分反应后向混合液中加入足量的氢氧化钠溶液,最终得到沉淀的质量为(单位:g)( )
| A、18 | B、20 | C、22 | D、24 |
下列说法不正确的是( )
| A、从氢核磁共振谱图上可以定量的分析出有机物中处于不同化学环境的氢原子的种类和比例 |
| B、红外光谱可以定性分析有机物中具有哪些基团或化学键 |
| C、李比希元素分析法能测得有机物中所有元素的质量分数 |
| D、钠熔融法和铜丝燃烧法都是定性检验有机物中某些特定元素的分析方法 |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、1.0 mo1?L-1的Na2CO3溶液中:c(OH-)═c(HCO3-)+c(H+)+c(H2CO3) |
| B、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、0.1 mol?L-1NaHCO3溶液中:c(Na+)>c(HCO3->c(CO32-)>c(H2CO3) |
| D、一定量(NH4)2SO4与NH3?H2O混合所得的酸性溶液中:c(NH4+)<2c(SO42-) |
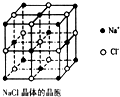 纳米材料的表面微 粒占总微粒数的比例极大,这是它有许多特殊性质的原因.假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数与总微粒数的比值为( )
纳米材料的表面微 粒占总微粒数的比例极大,这是它有许多特殊性质的原因.假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数与总微粒数的比值为( )| A、7:8 | B、13:14 |
| C、25:26 | D、26:27 |
高铁电池是一种新型可充电电池,电解质溶液为KOH,放电时的总反应式为3Zn+2K2FeO4+8H2O?3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是( )
| A、放电时负极反应为:3Zn-6e-+6OH-═3Zn(OH)2 |
| B、放电时OH-向正极移动 |
| C、充电时每转移3mol电子,阳极有1molFe(OH)3被还原 |
| D、充电时阳极反应式为:3Zn(OH)2+6e-═3Zn+6OH- |
要提取碘水中的碘,下列试剂不能成功的是( )
| A、CCl4 |
| B、苯 |
| C、汽油 |
| D、酒精 |