题目内容
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、C2H4 CH4 |
| B、CO2 H2 |
| C、C60 C2H4 |
| D、NH3 HCl |
考点:极性分子和非极性分子,极性键和非极性键
专题:
分析:非极性键为:同种元素的原子间形成的共价键;极性键为:不同元素的原子间形成的共价键;
极性分子为:正电荷中心和负电荷中心不相重合的分子;非极性分子:正电荷中心和负电荷中心相重合的分子;分子极性的判断方法为:分子的极性由共价键的极性及分子的空间构型两个方面共同决定.
极性分子为:正电荷中心和负电荷中心不相重合的分子;非极性分子:正电荷中心和负电荷中心相重合的分子;分子极性的判断方法为:分子的极性由共价键的极性及分子的空间构型两个方面共同决定.
解答:
解:A、C2H4中含有极性键和非极性键,是平面型分子,结构对称,分子中正负电荷重心重叠,为非极性分子,CH4 中含有极性键,为正四面体结构,结构对称,分子中正负电荷重心重叠,为非极性分子,故A正确;
B、二氧化碳为极性键形成的非极性分子,氢气为单质,不存在极性键,故B错误;
C、C60中只含有非极性键,为非极性分子;乙炔为极性键形成的非极性分子,故C错误;
D、氨气和氯化氢都是由极性键形成的分子,二者正电荷中心和负电荷中心不相重合,属于极性分子,故D错误.
故选:A.
B、二氧化碳为极性键形成的非极性分子,氢气为单质,不存在极性键,故B错误;
C、C60中只含有非极性键,为非极性分子;乙炔为极性键形成的非极性分子,故C错误;
D、氨气和氯化氢都是由极性键形成的分子,二者正电荷中心和负电荷中心不相重合,属于极性分子,故D错误.
故选:A.
点评:本题考查了键的极性和分子的极性判断,题目难度不大,侧重于对学生灵活运用基础知识解决实际问题的能力的培养.

练习册系列答案
相关题目
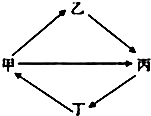 下列各组物质按如图所示转化关系每一个转化都能一步实现的是( )
下列各组物质按如图所示转化关系每一个转化都能一步实现的是( )| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | S | SO2 | H2SO4 | SO3 |
| B | CO2 | Na2CO3 | NaHCO3 | CaCO3 |
| C | N2 | HNO3 | NO2 | NH3 |
| D | SiO2 | Na2SiO3 | H2SiO3 | CaSiO3 |
| A、A | B、B | C、C | D、D |
下列各组粒子中属于同位素的是( )
| A、16O和18O |
| B、H2O和D2O |
| C、H2和D2 |
| D、24Mg和24Na |
下列防止金属腐蚀的做法不可行的是( )
| A、在某些工具的机械转动部位刷油漆 |
| B、在钢铁中加入铬 |
| C、在较小钢铁制品的表面包裹塑料 |
| D、在大型铁壳船的船身上装上一定数量的锌块 |
下列关于原电池的叙述中错误的是( )
| A、原电池是将化学能转变为电能的装置 |
| B、在原电池中,电子流出的一极是负极,发生氧化反应 |
| C、构成原电池的正极和负极必须是两种不同的金属 |
| D、在原电池中,电流的方向是从正极到负极 |
13 6 |
14 7 |
| A、质量数 | B、质子数 |
| C、电子数 | D、中子数 |
下列关于化学键的叙述中,正确的是( )
| A、离子键是阴、阳离子之间的静电引力 |
| B、物质中都含有化学键 |
| C、离子化合物中只含有离子键 |
| D、共价化合物中只含有共价键 |
下列含有共价键的化合物是( )
| A、MgCl2 |
| B、NaOH |
| C、Br2 |
| D、NaCl |

