题目内容
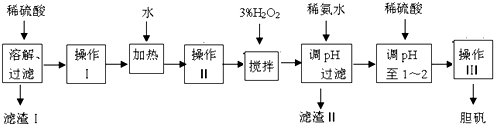
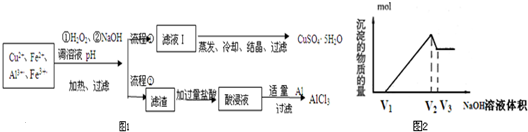
某研究小组将一批废弃的线路板经浓硝酸和稀硫酸处理后得到一混合溶液,其中含有Cu2+、Fe3+、Fe2+、Al3+等金属离子,并设计了以下两种流程以分别制取CuSO4?5H2O晶体和AlCl3溶液(如图1):流程
已知:相关金属离子开始沉淀至完全沉淀时的pH范围为:
请回答下列问题:
(1)加入H2O2的作用是 ,
(2)欲使制取的CuSO4?5H2O晶体较为纯净,pH至少应调至 ;
(3)写出H2O2在酸性条件下与Fe2+反应的离子方程式: ;
(4)根据你所学的化学知识,由AlCl3溶液(不添加其他化学试剂)能否制得无水AlCl3 (填:能或不能),原因是 ;
(5)取体积为V(L)的酸浸液,向其中滴加1mol?L-1的NaOH溶液,生成沉淀的物质的量与所加的NaOH溶液的体积(L)关系图2.请用V1、V2、V3表示所取的酸浸液中n(Fe3+):n(Al3+) .
已知:相关金属离子开始沉淀至完全沉淀时的pH范围为:
| 离子 | Fe3+ | Fe2+ | Al3+ | Cu2+ |
| pH范围 | 2.2~3.2 | 5.5~9.0 | 4.1~5.0 | 5.3~6.6 |
(1)加入H2O2的作用是
(2)欲使制取的CuSO4?5H2O晶体较为纯净,pH至少应调至
(3)写出H2O2在酸性条件下与Fe2+反应的离子方程式:
(4)根据你所学的化学知识,由AlCl3溶液(不添加其他化学试剂)能否制得无水AlCl3
(5)取体积为V(L)的酸浸液,向其中滴加1mol?L-1的NaOH溶液,生成沉淀的物质的量与所加的NaOH溶液的体积(L)关系图2.请用V1、V2、V3表示所取的酸浸液中n(Fe3+):n(Al3+)

考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:加H2O2把Fe2+氧化为Fe3+,加氢氧化钠调节pH,生成氢氧化铁和氢氧化铝沉淀,过滤得滤渣中含氢氧化铁和氢氧化铝,加过量盐酸生成氯化铝、氯化铁,酸浸液加入适量铝把铁置换出来,过滤得到氯化铝;对于滤液I,含硫酸铜,通过蒸发浓缩、冷却结晶、过滤洗涤得到硫酸铜晶体.
(1)加H2O2的作用是把Fe2+氧化为Fe3+,该氧化剂的优点是不引入杂质,产物对环境物污染;
(2)滤渣c是氢氧化铝,根据部分阳离子以氢氧化物形式沉淀时溶液的pH表,选择使氢氧化铝沉淀完全且氢氧化铜不沉淀的PH;
(3)双氧水具有氧化性,能够将亚铁离子氧化成铁离子;
(4)氯化铝属于强酸弱碱盐,会水解;
(5)根据图象结合反应原理进行计算.
(1)加H2O2的作用是把Fe2+氧化为Fe3+,该氧化剂的优点是不引入杂质,产物对环境物污染;
(2)滤渣c是氢氧化铝,根据部分阳离子以氢氧化物形式沉淀时溶液的pH表,选择使氢氧化铝沉淀完全且氢氧化铜不沉淀的PH;
(3)双氧水具有氧化性,能够将亚铁离子氧化成铁离子;
(4)氯化铝属于强酸弱碱盐,会水解;
(5)根据图象结合反应原理进行计算.
解答:
解:(1)第②步加H2O2的作用是将Fe2+氧化为Fe3+,过氧化氢做氧化剂不引入杂质,对环境无污染,故答案为:将Fe2+氧化为Fe3+,不引入杂质,产物对环境无污染;
(2)加入氢氧化钠溶液调节PH=x,目的是生成氢氧化铝沉淀,氢氧化铝开始沉淀PH=4,沉淀完全PH=5.0,氢氧化铜开始沉淀PH=5.4,所以选择的PH范围是:5.0≤X<5.4,pH至少应调至5.0,故答案为:5.0;
(3)亚铁离子被双氧水氧化成铁离子,反应的离子方程式为H2O2+2Fe2++2H+═2Fe3++2H2O,故答案为:H2O2+2Fe2++2H+═2Fe3++2H2O;
(4)氯化铝为强酸弱碱盐,水解反应方程式为:AlCl3+3H2O?Al(OH)3+3HCl水解为吸热反应,加热使水解平衡向水解方向移动,蒸干,氯化氢挥发,得到氢氧化铝,灼烧得到氧化铝;故答案为:不能;直接加热AlCl3溶液,会发生水解反应,最终得到氧化铝;
(5)0--V1阶段,滴加的NaOH用于中和剩余的HCl,发生反应是:HCl+NaOH=NaCl+H2O,
设Fe3+、Al3+物质的量分别为y、x,
V1--V2阶段,继续滴加的NaOH与Fe3+、Al3+反应:
Al3++3OH-=Al(OH)3↓,Fe3++3OH-=Fe(OH)3↓
x 3x x y 3y
则3x+3y=(V2-V1)×1
V2--V3阶段,继续滴加的NaOH与Al(OH)3反应,沉淀量开始减少,发生反应:
Al(OH)3+NaOH=NaAlO2+2H2O
x x
则x=(V3-V2)×1=V3-V2
y=
,
y:x=
,故答案为:
.
(2)加入氢氧化钠溶液调节PH=x,目的是生成氢氧化铝沉淀,氢氧化铝开始沉淀PH=4,沉淀完全PH=5.0,氢氧化铜开始沉淀PH=5.4,所以选择的PH范围是:5.0≤X<5.4,pH至少应调至5.0,故答案为:5.0;
(3)亚铁离子被双氧水氧化成铁离子,反应的离子方程式为H2O2+2Fe2++2H+═2Fe3++2H2O,故答案为:H2O2+2Fe2++2H+═2Fe3++2H2O;
(4)氯化铝为强酸弱碱盐,水解反应方程式为:AlCl3+3H2O?Al(OH)3+3HCl水解为吸热反应,加热使水解平衡向水解方向移动,蒸干,氯化氢挥发,得到氢氧化铝,灼烧得到氧化铝;故答案为:不能;直接加热AlCl3溶液,会发生水解反应,最终得到氧化铝;
(5)0--V1阶段,滴加的NaOH用于中和剩余的HCl,发生反应是:HCl+NaOH=NaCl+H2O,
设Fe3+、Al3+物质的量分别为y、x,
V1--V2阶段,继续滴加的NaOH与Fe3+、Al3+反应:
Al3++3OH-=Al(OH)3↓,Fe3++3OH-=Fe(OH)3↓
x 3x x y 3y
则3x+3y=(V2-V1)×1
V2--V3阶段,继续滴加的NaOH与Al(OH)3反应,沉淀量开始减少,发生反应:
Al(OH)3+NaOH=NaAlO2+2H2O
x x
则x=(V3-V2)×1=V3-V2
y=
| 4V2-V1-3V3 |
| 3 |
y:x=
| 4V2-V1-3V3 |
| 3(V3-V2) |
| 4V2-V1-3V3 |
| 3(V3-V2) |
点评:本题考查金属混合物的分离和提纯,关键是提取题中的信息和反应原理,根据所学知识完成,本题难度中等.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是( )
| A、烧杯中有铜无铁 |
| B、烧杯中有铁无铜 |
| C、烧杯中铁、铜都有 |
| D、烧杯中铁、铜都无 |
垃圾资源化的方法是( )
| A、填埋 | B、焚烧 |
| C、堆肥 | D、分类回收 |