题目内容
常温下,下列溶液中,有关微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1 (NH4)2Fe(SO4)2溶液: c(NH )> c(SO
)> c(SO )>c(Fe2+)>c(H+)
)>c(Fe2+)>c(H+)
B.0.1 mol·L-1 Na2CO3溶液:c(Na+)+c(H+)=c(CO )+c(HCO
)+c(HCO )+c(OH-)
)+c(OH-)
C.0.1 mol·L-1 NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(CO )
)
D.0.01 mol·L-1NaOH溶液与等体积pH=2的醋酸混合后的溶液中:c(CH3COO-)>c (Na+)>c(H+)> c (OH-)
D
【解析】
试题分析:A、0.1 mol·L-1 (NH4)2Fe(SO4)2溶液中,铵根离子、亚铁离子都发生水解,所以不水解的硫酸根离子的浓度最大,错误;B、根据电荷守恒规律,Na2CO3溶液中:c(Na+)+c(H+)=2c(CO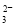 )+c(HCO
)+c(HCO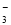 )+c(OH-),错误;C、0.1 mol·L-1 NaHCO3溶液中,根据质子守恒规律,c(OH-)= c(H+)+c(H2CO3)- c(CO
)+c(OH-),错误;C、0.1 mol·L-1 NaHCO3溶液中,根据质子守恒规律,c(OH-)= c(H+)+c(H2CO3)- c(CO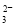 ),所以c(H+)+c(H2CO3)=c(OH-)+c(CO
),所以c(H+)+c(H2CO3)=c(OH-)+c(CO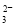 ),错误;D、pH=2的醋酸的浓度大于0.01mol/L,所以与0.01mol/L的NaOH溶液等体积混合时,醋酸过量,得到的醋酸与醋酸钠的混合液,所以溶液呈酸性,则c (CH3COO-) > c (Na+) > c (H+)> c (OH-),正确,答案选D。
),错误;D、pH=2的醋酸的浓度大于0.01mol/L,所以与0.01mol/L的NaOH溶液等体积混合时,醋酸过量,得到的醋酸与醋酸钠的混合液,所以溶液呈酸性,则c (CH3COO-) > c (Na+) > c (H+)> c (OH-),正确,答案选D。
考点:考查溶液中离子浓度的关系判断

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案实验室中某些气体的制取、收集及尾气处理装置如图所示。
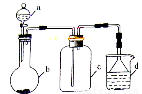
仅用此装置和表中提供的物质完成相关实验,最合理的是
选项 | a中物质 | b中物质 | c中收集的气体 | d中物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 饱和食盐水 | 电石 | CH≡CH | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
 2C(g),下列说法中正确的是
2C(g),下列说法中正确的是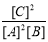
 2NO+O2,下列能作为反应达到平衡状态标志的是
2NO+O2,下列能作为反应达到平衡状态标志的是 rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分含量和温度T或压强P关系如图所示,下列叙述中正确的是
rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分含量和温度T或压强P关系如图所示,下列叙述中正确的是