题目内容
亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:__________Na2SO3+__________KIO3+__________H2SO4——______Na2SO4+__________K2SO4+__________I2+__________H2O
(1)配平上面的氧化还原反应方程式,将化学计量数填在空白处。
(2)其中氧化剂是__________,若反应中有5 mol电子转移,则生成的碘是__________ mol。
(3)该反应过程和机理较复杂,一般认分为以下①—④步反应:
①![]() +
+![]()
![]()
![]() +
+![]() (反应速率慢)
(反应速率慢)
②![]() +2
+2![]()
![]() I-+2
I-+2![]() (反应速率快)
(反应速率快)
③5I-+6H++![]()
![]() 3I2+3H2O (反应速率快)
3I2+3H2O (反应速率快)
④I2+![]() +H2O
+H2O![]() 2I-+
2I-+![]() +2H+ (反应速率快)
+2H+ (反应速率快)
根据上述条件推测,此反应总的反应速率由_________步反应决定(填上述4步反应的序号)。
(4)若预先加入淀粉溶液,由题述看必须在___________离子消耗完时,才会有使淀粉变蓝的现象产生。
解析:(1)利用氧化还原反应中,化合价升降总数相等配平方程式。
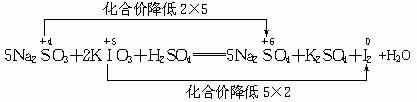
(2)氧化剂在反应中得电子,化合价降低,故为KIO3,每1 mol KIO3可得到5 mol电子,由碘原子守恒知,生成0.5 mol I2。
(3)化学反应速率由最慢的基元反应来决定。
(4)由第④步反应知,必须在![]() 消耗完时才会有使淀粉变蓝的现象产生。
消耗完时才会有使淀粉变蓝的现象产生。
答案:(1)5 2 1 5 1 1 1
(2)KIO3 0.5
(3)①
(4)![]()

练习册系列答案
相关题目
 杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。