题目内容
下列属于吸热反应的是( )
| A、中和反应 |
| B、金属与酸反应置换出H2 |
| C、燃烧反应 |
| D、炽热的炭与水蒸气反应制取水煤气 |
考点:吸热反应和放热反应
专题:
分析:根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答:
解:A.中和反应是放热反应,故A错误;
B.金属与酸反应置换出H2是常见放热反应,故B错误;
C.燃烧反应是放热反应,故C错误;
D.炽热的炭与水蒸气反应制取水煤气是吸热反应,故D正确.
故选D.
B.金属与酸反应置换出H2是常见放热反应,故B错误;
C.燃烧反应是放热反应,故C错误;
D.炽热的炭与水蒸气反应制取水煤气是吸热反应,故D正确.
故选D.
点评:本题考查吸热反应,难度不大,掌握中学化学中常见的吸热或放热的反应是解题的关键.

练习册系列答案
相关题目
下列叙述中错误的是( )
| A、电解池是电能转化为化学能的装置 |
| B、原电池跟电解池连接后,电子从原电池负极流向电解池阳极 |
| C、电镀时,电镀池里的阳极材料发生氧化反应 |
| D、用惰性电极电解饱和食盐水时,阴极得到氢氧化钠溶液和氢气 |
如图是198K时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
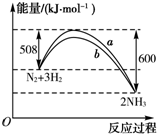

| A、该反应的热化学方程式为N2+3H2?2NH3△H=-92 kJ?mol-1 |
| B、a曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的反应热改变 |
| D、升高温度,反应速率加快 |
下列反应属于吸热反应的是( )
| A、2Mg十O2=2MgO |
| B、C十H2O=CO十H2 |
| C、HCl十NaOH=NaCl十H2O |
| D、CaO十H2O=Ca(OH)2 |
关于离子键、共价键的各种叙述,下列说法中正确的是( )
| A、在离子化合物里,只存在离子键,没有共价键 |
| B、任何分子中一定都存在化学键 |
| C、在共价化合物分子内,一定不存在离子键 |
| D、全部由非金属元素形成的化合物中不可能含有离子键 |
如图是从元素周期表中截取下来的,A、B、C为短周期主族元素,下列有关叙述正确的是( )


| A、D一定是金属元素,其金属性比C强 |
| B、C的最高价氧化物对应的水化物一定显强酸性 |
| C、B的氢化物一定是分子晶体,晶体中一定存在氢键 |
| D、E的原子序数一定是A的5倍,且原子半径比A大 |
下列热化学方程式中,△H能正确表示物质的燃烧热或中和热的是( )
| A、2H2(g)+O2(g)═2H2O(l)△H═-572kJ?mol-1 |
| B、KOH(aq)+CH3COOH (aq)=CH3COOK (aq)+H2O(l);△H=-57.3 kJ?mol-1 |
| C、C8H18(l)+12.5O2 (g)=8CO2(g)+9H2O(l);△H=-5518 kJ?mol-1 |
| D、CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H═-533kJ?mol-1 |