题目内容
工业制纯碱的第一步是通过饱和食盐水、氨和二氧化碳之间的反应,制取碳酸氢钠晶体。该反应原理可以用以下化学方程式表示,已知此反应是放热反应。
NH3+CO2+H2O+NaCl(饱和)= NaHCO3(晶体)↓+NH4Cl
(1)利用上述反应原理,设计如下图所示装置,制取碳酸氢钠晶体.B中盛有饱和碳酸氢钠溶液,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去.制取碳酸氢钠晶体可供选用的药品有:a.石灰石 b.生石灰 c.6mol/L盐酸 d.稀硫酸
e.浓氨水 f.饱和氯化钠溶液。
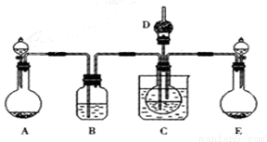
①A中制备气体时,所需药品是(选填字母代 号) ;
①B中盛有饱和碳酸氢钠溶液,其作用是 ;
③在实验过程中,向C中通入气体是有先后顺序的,应先通入气体的化学式为 ;
④E装置向C中通气的导管不能插入液面下的原因是 。
(2)该小组同学为了测定C中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是(选填字母序号) ;
A.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
B.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
C.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②操作Ⅲ的方法为 、 、 ;
③所得晶体中碳酸氢钠的纯度为 。
(12分)
(1)ac(少写得一分,错写都不得分)(2分) 除二氧化碳中的氯化氢(1分)
NH3(1分) 防止倒吸(1分)
(2)A(2分) 过滤,洗涤,干燥(3分) 168n/(100w)(答案合理都给分)(2分)
【解析】
试题分析:(1)因为B中盛有饱和碳酸氢钠溶液,所以B装置的作用应是除去二氧化碳中的氯化氢气体,所以A装置是制取二氧化碳的装置,应选择石灰石与稀盐酸,答案选ac;B的作用就是除去二氧化碳中的氯化氢气体;E装置是产生氨气的装置,在该实验中未增大二氧化碳的吸收量,应先通入氨气,使溶液呈碱性再通入二氧化碳气体;E装置向C中通气的导管不能插入液面以下是因为生石灰溶于水放热,氨气极易溶于水,若插入液面以下会发生倒吸,使烧瓶炸裂;
(2)①A、在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,应向溶液中再加入氯化钙溶液,若仍有沉淀生成,说明氯化钙不足,若无沉淀生成说明氯化钙已过量,正确;B、若滴加碳酸钠溶液,虽然能够判断氯化钙是否过量,但是给实验带来干扰,n值增大,错误;C、在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液,可以判断氯化钙是否过量,但相比较A而言,步骤繁琐,所以最佳答案选A;
②操作II中得到碳酸钙沉淀,到称量碳酸钙固体,需要先将碳酸钙过滤,然后洗涤、干燥后再称量;
③碳酸钙的质量是ng,物质的量是n/100mol,则碳酸钠的物质的量也是n/100mol,则样品中碳酸氢钠的物质的量是2n/100mol,则wg样品中碳酸氢钠的质量分数是2n/100mol×84g/mol/wg×100%= 168n/(100w),或者是168n/w%。
考点:考查化学工艺流程的分析及基本实验操作的应用,质量分数的计算

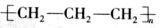


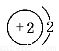 C.1s2 D.
C.1s2 D.
 B . CO2 C . Na2O2 D . NH4Cl
B . CO2 C . Na2O2 D . NH4Cl B.
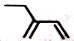
B.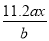 C.
C. D.
D.
 ,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是( )。
,ZX2是一种储氢材料,W与Y属于同一主族,下列叙述正确的是( )。