题目内容
12.某烃的密度在标况下是2.59g/L,此烃分子中含碳82.8%,写出该烃的分子式C4H10.分析 结合M=ρVM、此烃分子中含碳82.8%,计算出C、H原子个数比,以此得到化学式.
解答 解:烃的密度在标况下是2.59g/L,M=22.4L/mol×2.59g/L=58g/mol,
此烃分子中含碳82.8%,
则C、H原子个数比为$\frac{82.8%}{12}$:$\frac{1-82.8%}{1}$=2:5,
设烃分子式为C2nH5n,则12×2n+1×5n=58,解得n=2,
即该烃的分子式为C4H10,
故答案为:C4H10.
点评 本题考查有机物分子式确定的计算,为高频考点,把握物质的量的相关计算公式、分子式中原子个数比的计算方法等为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
2.由二氧化硅制高纯硅的流程如下,下列判断中不正确的是( )

| A. | ①②③均属于氧化还原反应 | B. | H2和HCl均可循环利用 | ||
| C. | SiO2是一种坚硬难熔的固体 | D. | 硅可用于制作光导纤维 |
3.在下列各组离子中,能大量共存的且溶液呈无色是( )
| A. | Na+、H+、Al3+、CH3COO- | B. | Mg2+、HCO3-、Ca2+、NO3- | ||
| C. | K+、SO42-、Cl-、Cu2+ | D. | NH4+、Cl-、K+、OH- |
20.当今人类利用的常规能源是( )
| A. | 化石燃料 | B. | 太阳能 | C. | 核能 | D. | 潮汐能 |
7.有机化合物R的结构简式为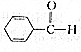 ,R的同分异构体中属于芳香化合物并能跟钠反应的种类有( )
,R的同分异构体中属于芳香化合物并能跟钠反应的种类有( )
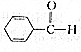 ,R的同分异构体中属于芳香化合物并能跟钠反应的种类有( )
,R的同分异构体中属于芳香化合物并能跟钠反应的种类有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
4.下列各组物质中属于同分异构体的是( )
| A. |  和 和 | B. |  与 与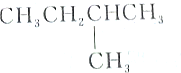 | ||
| C. |  与 与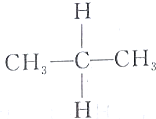 | D. |  与 与 |
14.在标准状况下进行甲、乙、丙三组实验.三组实验均各取20mL同浓度的盐酸,加入同一种镁铝合金粉末,产生气体,有关数据见下表:
请回答下列问题:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?乙(填“甲”或“乙”).理由是因甲反应后的溶液中再加合金还能继续反应,说明甲中盐酸有剩余,若乙中盐酸恰好完全反应或有剩余,则产生的氢气应为$\frac{385}{255}$×280mL=423mL>336mL,故说明乙中盐酸不足.
(2)要算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得的盐酸的物质的量浓度为1.5mol/L.
(3)求合金中Mg、Al的物质的量之比,题中可作为计算依据的数据是甲,求得的Mg、Al物质的量之比为1:1.
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 255 | 385 | 459 |
| 生成气体体积/mL | 280 | 336 | 336 |
(1)甲、乙两组实验中,哪一组盐酸是不足量的?乙(填“甲”或“乙”).理由是因甲反应后的溶液中再加合金还能继续反应,说明甲中盐酸有剩余,若乙中盐酸恰好完全反应或有剩余,则产生的氢气应为$\frac{385}{255}$×280mL=423mL>336mL,故说明乙中盐酸不足.
(2)要算出盐酸的物质的量浓度,题中可作为计算依据的数据是乙或丙,求得的盐酸的物质的量浓度为1.5mol/L.
(3)求合金中Mg、Al的物质的量之比,题中可作为计算依据的数据是甲,求得的Mg、Al物质的量之比为1:1.
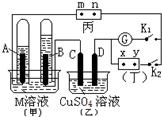 如图所示的实验装置,丙为酚酞溶液润湿的淀粉碘化钾试纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A极产生的气体体积为44.8ml、B极产生的气体体积为22.4ml(都已换算成标况下的体积),回答下列问题:
如图所示的实验装置,丙为酚酞溶液润湿的淀粉碘化钾试纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1,一段时间后,A极产生的气体体积为44.8ml、B极产生的气体体积为22.4ml(都已换算成标况下的体积),回答下列问题: