题目内容
 向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2(其中,甲充入2mol SO2、1mol O2,乙充入1mol SO2、0.5mol O2),发生反应:2SO2(g)+O2(g)?2SO3(g);△H=-197.74kJ?mol-1.
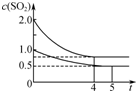
向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2(其中,甲充入2mol SO2、1mol O2,乙充入1mol SO2、0.5mol O2),发生反应:2SO2(g)+O2(g)?2SO3(g);△H=-197.74kJ?mol-1.一段时间后达到平衡,测得两容器中c(SO2)(mol?L-1)随时间t(min)的变化关系如图所示.下列说法正确的是( )
| A、热量:Q(甲)<2Q(乙) |
| B、压强:p(甲)<2p(乙) |
| C、乙中前5 min内的反应速率v(O2)=0.10 mol?L-1?min-1 |
| D、保持其他条件不变,若起始时向乙中充入0.4 mol SO2、0.2 mol O2、0.4 mol SO3,则此时v(正)<v(逆) |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,据此分析热量关系;
B.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,据此分析压强大小;
C.计算乙中前5 min内SO2浓度变化得到v(O2);
D.利用浓度商与化学平衡常数比较判断.
B.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,据此分析压强大小;
C.计算乙中前5 min内SO2浓度变化得到v(O2);
D.利用浓度商与化学平衡常数比较判断.
解答:
解:A.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,放出热量Q(甲)>2Q(乙),故A错误;
B.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,则压强p(甲)<2p(乙),故B正确;
C.乙中前5 min内SO2浓度变化为1mol/L-0.5mol/L-0.5mol/L,v(SO2)=
=0.10mol/(L?min),则v(O2)=
×v(SO2)=0.0510mol/(L?min),故C错误;
D.乙容器达到化学平衡状态时,SO2浓度为0.5mol/L,O2浓度为:0.5mol/L-
×0.5mol/L=0.25mol/L,SO3浓度等于SO2浓度变化为0.5mol/L,K=
=4,浓度商为:
=5,浓度商大于化学平衡常数,化学平衡向逆反应方向移动,即v(正)<v(逆),故D正确;
故选BD.
B.该反应反应前气体体积大于反应后体积,即充入反应物物质的量越大则压强越大,进行程度较大,则压强p(甲)<2p(乙),故B正确;
C.乙中前5 min内SO2浓度变化为1mol/L-0.5mol/L-0.5mol/L,v(SO2)=
| 0.5mol/L |
| 5min |
| 1 |
| 2 |
D.乙容器达到化学平衡状态时,SO2浓度为0.5mol/L,O2浓度为:0.5mol/L-
| 1 |
| 2 |
| (0.5mol/L)2 |
| (0.5mol/L)2?0.25mol/L |
| (0.4mol/L)2 |
| (0.4mol/L)2?0.2mol/L |
故选BD.
点评:本题考查化学平衡图象、影响平衡的因素、化学反应速率的计算等,难度不大.

练习册系列答案
相关题目
化学与生活密切相关,下列有关说法正确的是( )
| A、只用淀粉溶液就可鉴别市售食盐是否为加碘盐 |
| B、淀粉、蚕丝、油脂都属于天然高分子化合物 |
| C、糖类、油脂和蛋白质都是人体所需基本营养物质,都能发生水解反应 |
| D、一定条件下,由葡萄糖可以制得酒精 |
 央视“315特别行动”曝光了河南一些地方“瘦肉精”事件.“瘦肉精”对人体健康会产生危害.已知某种“瘦肉精”含有克伦特罗(Clenbuterol),其结构如图.下列有关克伦特罗的叙述,正确的是( )
央视“315特别行动”曝光了河南一些地方“瘦肉精”事件.“瘦肉精”对人体健康会产生危害.已知某种“瘦肉精”含有克伦特罗(Clenbuterol),其结构如图.下列有关克伦特罗的叙述,正确的是( )| A、该物质的分子式为C12H17ON2Cl |
| B、该物质不溶于盐酸 |
| C、该物质能与FeCl3溶液发生显色反应 |
| D、该物质分子间都可以形成氢键 |
下列事实中,能说明氯的非金属性比硫强的是( )
①HClO的氧化性比H2SO4的氧化性强
②常温下氯气是气态而硫是固态
③盐酸酸性比氢硫酸强
④HCl比H2S稳定
⑤H2S能被Cl2氧化成硫
⑥SCl2分子中氯显-1价
⑦氯气与氢气化合比硫与氢气化合要容易进行
⑧Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
①HClO的氧化性比H2SO4的氧化性强
②常温下氯气是气态而硫是固态
③盐酸酸性比氢硫酸强
④HCl比H2S稳定
⑤H2S能被Cl2氧化成硫
⑥SCl2分子中氯显-1价
⑦氯气与氢气化合比硫与氢气化合要容易进行
⑧Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
| A、①②③④⑤⑥⑦⑧ |
| B、①④⑤⑥⑦ |
| C、④⑤⑥⑦⑧ |
| D、③④⑤⑦⑧ |
下列判断中,正确的是( )
| A、工业上常通过电解熔融的MgO冶炼金属镁 |
| B、将NaOH溶液逐滴加入FeCl3溶液可制备Fe(OH)3胶体 |
| C、牡丹籽油是一种优良的植物油脂,它可使酸性高锰酸钾溶液褪色 |
| D、溴水不能区别四种有机溶剂:苯、四氯化碳、己烯、无水乙醇 |
某同学按如图所示的装置进行实验,A、B为常见金属,它们的硫酸盐可溶于水.当K闭合时,X电极附近溶液先变红.下列分析不正确的是( )
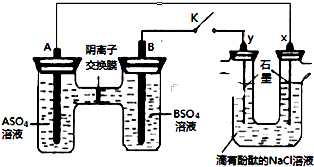

| A、A的金属活动性强于B |
| B、Y的电极反应:2Cl--2e-═Cl2↑ |
| C、阴离子交换膜处的SO42-从左向右移动 |
| D、当电路中有0.1mol电子通过时B电极有0.05mol金属析出 |
下列说法正确的是( )
| A、不锈钢是铁合金,只含有金属元素 |
| B、木糖醇(C5H10O5)是一种甜味剂,它属于多羟基化合物,与葡萄糖是同分异构体 |
| C、蛋白质在体内经消化后生成碳酸、硫酸、尿酸等,故它属于酸性食物 |
| D、氟氯代烷化学性质稳定,在紫外线照射下分解出氯原子参与破坏臭氧层的反应 |
常温下,铁与下列酸溶液作用产生H2的是( )
| A、硅酸 | B、浓硫酸 |
| C、稀盐酸 | D、稀硝酸 |
关于“植物油”的叙述错误的是( )
| A、属于酯类 |
| B、不含碳碳双键 |
| C、比水轻 |
| D、在碱和加热条件下能完全水解 |