题目内容
10.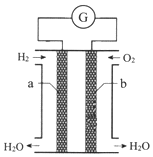 氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是( )
氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是( )| A. | a电极是该电池的正极 | |
| B. | 电池工作时,电从a电极流出经导线流向b电极 | |
| C. | 工作一段时间后,电解质溶液碱性减弱 | |
| D. | b极的电极反应式为:O2+2H2O+4e-═4OH- |
分析 氢氧燃料碱性电池中,负极上通入燃料,燃料失电子和氢氧根离子反应生成水,正极上通入氧气,氧气得电子和水反应生成氢氧根离子,据此分析解答.
解答 解:A.a电极上氢气失电子,则a是该电池的负极,故A错误;
B.原电池中电子从负极流向正极,即从a电极流出经导线流向b电极,故B正确;
C.该电池的总反应是氢气与氧气反应生成水,溶液的体积增大,氢氧根离子浓度减小,则电解质溶液碱性减弱,故C正确;
D.b极上氧气得电子生成氢氧根离子,电极反应式为:O2+2H2O+4e-═4OH-,故D正确;
故选A.
点评 本题考查了燃料电池,明确各个电极上发生的反应即可解答,注意电极反应式的书写与溶液酸碱性有关,该燃料电池中,酸性条件下不能生成氢氧根离子、碱性条件下不能生成氢离子,为易错点.

练习册系列答案
相关题目
6.表中,对陈述Ⅰ、Ⅱ的正确性判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 碳酸钠、碳酸氢钠能用澄清石灰水鉴别 | Na2CO3能与澄清石灰水反应生成白色沉淀, 而NaHCO3不能 |
| B | 金属钠具有强还原性 | 高压钠灯发出透雾性强的红光 |
| C | Cl2和SO2都具有漂白性 | Cl2和SO2混合用于漂白纸张 |
| D | 用浓H2SO4吸收SO3 | SO3能和水反应 |
| A. | A | B. | B | C. | C | D. | D |
1.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 在常温常压下,28gN2与CO混合物气体中所含的分子数目一定为NA | |
| B. | 标准状况下,17g氨气所含原子数目为NA | |
| C. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| D. | NA个氢分子所占有的体积一定为22.4L |
18.下列改变可确认化学平衡一定移动的是( )
| A. | 化学平衡常数发生了改变 | |
| B. | 有气态物质参加的可逆反应达到平衡后,改变了压强 | |
| C. | 正逆反应速率发生了改变 | |
| D. | 有固态物质参加的可逆反应达到平衡后,移走适量的固态物质 |
5.未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且可以再生.下列最有希望的新能源是( )①天然气 ②煤 ③石油 ④太阳能 ⑤氢能.
| A. | ①③⑤ | B. | ②③④ | C. | ①④⑤ | D. | ④⑤ |
15.下列属于碱的是( )
| A. | H2SO4 | B. | KOH | C. | Na2CO3 | D. | Na2O |
2.将某无色气体X通入品红溶液,溶液褪色;加热,溶液又变红色,X可能是( )
| A. | O2 | B. | Cl2 | C. | SO2 | D. | CO2 |
19.能说明某温度下,反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在密闭容器中,已达到平衡状态的是( )
| A. | NH3、NO消耗的速率相等 | |
| B. | 容器内NH3、O2、NO、H2O四种气体共存 | |
| C. | NO、H2O的生成速率相等 | |
| D. | 单位时间内NH3、O2消耗的物质的量相等 |