题目内容
 在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据:
在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析得到如下数据:| 时间(s) n(mol) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算20s~40s内用N2O4表示的平均反应速率为
(3)在一定温度下上述反应达到平衡的标志是
A.容器中压强不变
B.容器内c(N2O4):c(NO2)=1:2
C.混合气体中c(NO2)不变
D.单位时间消耗1摩尔N2O4的同时生成2摩尔的NO2
(4)反应进行至100s后将反应混合物的温度降低,混合气体的颜色
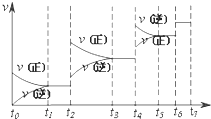
(5)达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图:若不改变(N2O4、NO2的量,则图中t4时引起平衡移动的条件可能是
考点:化学平衡的计算,化学平衡的影响因素,化学平衡状态的判断
专题:化学平衡专题
分析:(1)化学平衡常数表达式等于生成物浓度的幂之积比上反应物浓度的幂之积,由表中数据可知80s时,反应达平衡状态,计算出平衡时反应混合物各组分的物质的量,进而计算平衡时各组分的浓度,代入平衡常数表达式计算;
(2)20s~40s内用N2O4表示的平均反应速率为V=
;
(3)正逆速率相等,各组分的浓度保持不变的状态;
(4)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小;
(5)根据图象中曲线的走向综合分析解决.
(2)20s~40s内用N2O4表示的平均反应速率为V=
| △C |
| △t |
(3)正逆速率相等,各组分的浓度保持不变的状态;
(4)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小;
(5)根据图象中曲线的走向综合分析解决.
解答:
解:(1)化学平衡常数表达式等于生成物浓度的幂之积比上反应物浓度的幂之积,K=
,由表中数据可知80s时,反应达平衡状态,由(1)中计算可知d=e=0.1mol,故c(N2O4)=
=0.05mol/L,c(NO2)=
=0.3mol/L,所以该温度下平衡常数k=
mol?L-1=1.8mol?L-1,
故答案为:K=
;1.8;
(2)N2O4(g)?2NO2(g)
初起:0.40mol 0
20s后:a 0.24mol
b=0.40mol-0.24mol÷2=0.28mol,
20s~40s内用N2O4表示的平均反应速率为V=
=
=0.002mol/(L?s),
故答案为:0.002mol/(L?s);
(3)A.容器中压强不变,说明正逆速率相等,达平衡状态,故选;
B.容器内c(N2O4):c(NO2)=1:2,并不是不变的状态,故不选;
C.混合气体中c(NO2)不变,说明正逆速率相等,达平衡状态,故选;
D.单位时间消耗1摩尔N2O4的同时生成2摩尔的NO2,从反应开始到平衡的建立者有这样的关系,所以不一定平衡,故不选;
故答案为:AC;
(4)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小,气体的颜色变浅,故答案为:变浅;
(5)由题目要求只是改变某一外界条件,结合图象,可知t4时正逆反应速率都变大,而平衡逆向移动,可能增大压强,或缩小体积,t6时反应速率加快,但平衡不移动,而且两边的化学计量数不等,只能是加入了催化剂,图中表示平衡混合气体中NO2的含量最高的一段时间是,平衡一直正向移动后的平衡状态,即:t3~t4,
故答案为:缩小体积;加入了催化剂;t3~t4.
| c2(NO2) |
| c(N2O4) |
| 0.1mol |
| 2L |
| 0.6mol |
| 2L |
| 0.32 |
| 0.05 |
故答案为:K=
| c2(NO2) |
| c(N2O4) |
(2)N2O4(g)?2NO2(g)
初起:0.40mol 0
20s后:a 0.24mol
b=0.40mol-0.24mol÷2=0.28mol,
20s~40s内用N2O4表示的平均反应速率为V=
| △C |
| △t |
| ||
| 40s-20s |
故答案为:0.002mol/(L?s);
(3)A.容器中压强不变,说明正逆速率相等,达平衡状态,故选;
B.容器内c(N2O4):c(NO2)=1:2,并不是不变的状态,故不选;
C.混合气体中c(NO2)不变,说明正逆速率相等,达平衡状态,故选;
D.单位时间消耗1摩尔N2O4的同时生成2摩尔的NO2,从反应开始到平衡的建立者有这样的关系,所以不一定平衡,故不选;
故答案为:AC;
(4)该反应正反应是吸热反应,降低温度平衡向逆反应方向移动,NO2浓度减小,气体的颜色变浅,故答案为:变浅;
(5)由题目要求只是改变某一外界条件,结合图象,可知t4时正逆反应速率都变大,而平衡逆向移动,可能增大压强,或缩小体积,t6时反应速率加快,但平衡不移动,而且两边的化学计量数不等,只能是加入了催化剂,图中表示平衡混合气体中NO2的含量最高的一段时间是,平衡一直正向移动后的平衡状态,即:t3~t4,
故答案为:缩小体积;加入了催化剂;t3~t4.
点评:本题考查化学平衡移动及计算、反应热计算、原电池、盐类水解等,题目较为综合,具有一定难度,做题时注意外界条件对化学平衡的影响,注意(1)④中平衡常数只受温度影响,温度不变平衡常数不变.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
下列离子方程式书写正确的是( )
| A、碳酸钙溶于醋酸溶液中:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氯化镁溶液和氨水混合:Mg2++2OH-=Mg(OH)2 |
| C、铁与稀硫酸反应:2Fe+6H+═2Fe3++H2↑ |
| D、铜片插入硝酸银溶液中 Cu+2Ag+=Cu2++2Ag |
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、常温下.5.6克Fe投入到浓硝酸中,生成0.1NA的Fe3+ |
| B、0.1 mol的白磷(P4)或甲烷分子中所含的共价键数均为0.4NA |
| C、在精炼铜或电镀铜的过程中,当阴极都析出32 g铜时转移电子数均为NA |
| D、通过MnO2催化使H2O2分解,产生32g O2时转移电子数为4NA |
只用下列一种试剂就可以将六种无色液体:C2H5OH、AgNO3溶液、C2H5Br、苯酚溶液、己烯、苯鉴别开来的是( )
| A、FeCl2溶液 |
| B、溴水 |
| C、酸性高锰酸钾溶液 |
| D、NaOH溶液 |