题目内容
设NA为阿佛加德罗常数的数值,下列说法不正确的是( )
| A、常温常压下,1.7g NH3含有NA个电子 |
| B、标准状况下,22.4L水中含H2O分子NA个 |
| C、1molNa完全反应生成NaCl时,失去NA个电子 |
| D、常温常压下,22.4LCO2中含有的CO2分子数小于NA个 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据氨气的质量计算出氨气的物质的量及含有的电子数;
B、标况下,水为液态;
C、根据反应后钠元素的价态来分析;
D、常温常压下,气体摩尔体积大于22.4L/mol.
B、标况下,水为液态;
C、根据反应后钠元素的价态来分析;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答:
解:A、1.7g氨气的物质的量为0.1mol,1mol氨气含有10mol电子,故0.1mol氨气含有的电子数目为NA,故A正确;
B、标况下,水为液态,故B错误;
C、反应后钠元素的价态为+1价,故1mol钠失去1mol电子,为NA个,故C正确;
D、常温常压下,气体摩尔体积大于22.4L/mol,故二氧化碳的物质的量小于1mol,分子个数小于NA个,故D正确.
故选B.
B、标况下,水为液态,故B错误;
C、反应后钠元素的价态为+1价,故1mol钠失去1mol电子,为NA个,故C正确;
D、常温常压下,气体摩尔体积大于22.4L/mol,故二氧化碳的物质的量小于1mol,分子个数小于NA个,故D正确.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2SO2(g)+O2(g)
2SO3(g)是制备硫酸的重要反应.下列叙述正确的是( )
| v2o5 |
| △ |
| A、催化剂V2O5不改变该反应的逆反应速率 | ||
| B、增大反应体系的压强,反应速率一定增大 | ||
| C、该反应是放热反应,降低温度将缩短反应达到平衡的时间 | ||
D、在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率v=
|
下列两分子的关系是( )
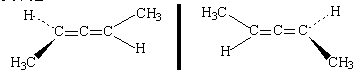
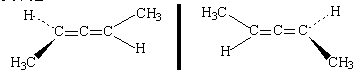
| A、互为同素形体 |
| B、同一物质 |
| C、手性异构体 |
| D、互为同系物 |
下列有关溶液和胶体的叙述正确的是( )
| A、Fe(OH)3胶体和FeCl3溶液区别的本质特征为是否具有丁达尔效应 |
| B、FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷 |
| C、纳米材料的微粒直径一般从几纳米到几十纳米,因此纳米材料是胶体 |
| D、FeCl3溶液能使血液凝聚沉降 |
设NA为阿伏加德罗常数,在标准状况下,下列说法正确的是( )
| A、60g水晶晶体中,含有“Si-O”键的数目为2NA |
| B、14g氮气含有π键数为2NA |
| C、18g冰中含有的氢键数目为2NA |
| D、12g金刚石中含有C-C键的数目为4NA |
 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示.下列叙述错误的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的NaOH溶液,所加NaOH溶液的体积与产生沉淀的物质的量关系如图所示.下列叙述错误的是( )| A、x与y的差值为0.01mol |
| B、原溶液中c(Cl-)=0.85mol?L-1 |
| C、原溶液的c(H+)=0.1mol?L-1 |
| D、原溶液中n(Mg2+):n(Al3+)=5:1 |
用蒸馏水湿润过的pH试纸测得某氨基酸溶液的pH等于8,则该氨基酸溶液的pH可能是( )
| A、9 | B、8 | C、7 | D、6 |
钠元素在自然界存在的主要形式为( )
| A、金属钠 |
| B、NaOH |
| C、NaCl |
| D、Na2CO3 |