题目内容
欲除去下列物质中的杂质(括号内为杂质)所用试剂和操作方法都正确的是( )
①Cl2(HCl):饱和食盐水、过滤
②NaHCO3溶液(Na2CO3):通入过量的CO2气体
③铁粉(铝粉):NaOH、过滤
④MnO2(KCl):水、溶解后过滤
⑤碳粉(碘单质):CCl4、分液.
①Cl2(HCl):饱和食盐水、过滤
②NaHCO3溶液(Na2CO3):通入过量的CO2气体
③铁粉(铝粉):NaOH、过滤
④MnO2(KCl):水、溶解后过滤
⑤碳粉(碘单质):CCl4、分液.
| A、①②③ | B、②④⑤ |
| C、②③④ | D、①④⑤ |
考点:物质的分离、提纯和除杂
专题:化学实验基本操作
分析:①HCl极易溶于水,利用洗气法除杂;
②CO2能与饱和Na2CO3溶液反应;
③Al与NaOH溶液反应,而Fe不反应;
④KCl溶于水,而MnO2不溶于水;
⑤碘易溶于CCl4,而碳粉不溶.
②CO2能与饱和Na2CO3溶液反应;
③Al与NaOH溶液反应,而Fe不反应;
④KCl溶于水,而MnO2不溶于水;
⑤碘易溶于CCl4,而碳粉不溶.
解答:
解:①HCl极易溶于水,则除去Cl2中的HCl,可通过盛有饱和食盐会的洗气瓶即可,故①错误;
②CO2能与饱和Na2CO3溶液反应生成碳酸氢钠,故②正确;
③Al与NaOH溶液反应,而Fe不反应,则除去Fe中的Al,通过NaOH溶液后过滤即可,故③正确;
④KCl溶于水,而MnO2不溶于水,则除去二氧化锰中的KCl,溶于水后过滤即可,故④正确;
⑤碘易溶于CCl4,而碳粉不溶,则除去碳粉中的碘,加四氯化碳后过滤,故⑤错误;
故选C.
②CO2能与饱和Na2CO3溶液反应生成碳酸氢钠,故②正确;
③Al与NaOH溶液反应,而Fe不反应,则除去Fe中的Al,通过NaOH溶液后过滤即可,故③正确;
④KCl溶于水,而MnO2不溶于水,则除去二氧化锰中的KCl,溶于水后过滤即可,故④正确;
⑤碘易溶于CCl4,而碳粉不溶,则除去碳粉中的碘,加四氯化碳后过滤,故⑤错误;
故选C.
点评:本题考查混合物的分离、提纯,明确物质的性质是解答本题的关键,注意两种物质的性质差异及除杂的原则来解答,题目难度不大.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
下列反应中,属于加成反应的是( )
| A、CH2=CH2+HCl→CH3CH2Cl | |||
B、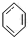 +HO-NO2 +HO-NO2
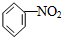 +H2O +H2O | |||
C、CH4+Cl2
| |||
D、2 CH3CH2OH+O2
|
实验是化学学习的基础.下列实验叙述正确的是( )
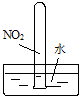 | 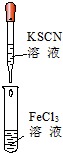 | 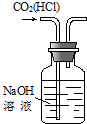 | 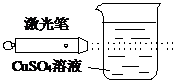 |
| ① | ② | ③ | ④ |
| A、实验①试管最终会充满水 |
| B、实验②试管中溶液变为血红色 |
| C、可用实验③装置除去CO2气体中含有的少量HCl杂质 |
| D、实验④CuSO4溶液中会形成一条光亮的通路 |
向11.2g Fe2O3、Cu的混合物中加入0.25mol?L-1的硫酸溶液600mL时,固体恰好完全溶解,溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A、2.4g | B、1.6g |
| C、4.8g | D、6.4g |
实验室用锌粒与2mol?L-1硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )
| A、向该硫酸溶液中加入少量浓硫酸 |
| B、向该硫酸溶液中加入少量水 |
| C、改用热的2 mol?L-1硫酸溶液 |
| D、用锌粉代替锌粒 |
将BaCl2溶液分盛在两支试管中,第1支加入HNO3,第2支加入烧碱溶液,然后再分别通入SO2气体,结果两试管均有白色沉淀产生.下列说法正确的是( )
| A、证明SO2具有强氧化性和酸性 | ||
| B、若第1支试管改通H2S或Cl2气体,后再通SO2气体,均不会产生沉淀 | ||
| C、若第2支试管改通NH3,后通SO2,不会产生沉淀 | ||
D、升高pH使SO2水溶液中SO
|
在2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O的反应中,未被氧化的HCl与被氧化的HCl的物质的量之比是( )
| A、16:5 | B、2:5 |
| C、1:4 | D、3:5 |
下列反应属于氧化还原反应的是( )
| A、Na2O+H2O═2NaOH | ||||
| B、CuSO4+Fe═Cu+FeSO4 | ||||
| C、K2CO3+2HCl═2KCl+H2O+CO2↑ | ||||
D、NH4Cl
|
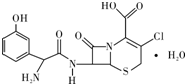 头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是( )
头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是( )| A、其分子式可以表示为C15H16ClN3O6S |
| B、该物质具有两性 |
| C、1 mol该化合物与NaOH溶液作用时消耗NaOH的物质的量最多为 4 mol |
| D、该物质的分子结构中有3个手性碳原子 |